一、科学性与思想性统一的原则
中学化学教学中的科学性,主要是指化学教学内容必须是符合现代科学水平的,反映客观事实、正确、可靠、系统的化学科学知识与技能。
中学化学教学中的思想性,主要是指在中学化学教学中坚持贯彻使学生德、智、体全面发展和保证中学教育“双重”任务的教学方向,化学教学内容中包含着对学生进行政治思想教育的因素,以及用马克思主义的立场、观点和方法阐明教学内容。
在教学中,既要反对空喊政治口号而破坏科学知识、技能教学的倾向, 又要反对只强调科学知识、技能教学而忽视思想教育的倾向,应该坚持实现思想性和科学性的统一。既教书又育人。这是培养有社会主义觉悟的有文化的劳动者的要求,体现了我国教学的根本方向和性质。为此,教师必须深入钻研化学教材的科学内容和思想内容,并在教学过程中把二者有机地结合起来。讲授时,要注意用正确无误的语言予以表达。
在中学化学教学中,结合化学科学知识教学进行思想教育的内容是很丰富的。例如,在绪言课里,以及各章节的教学中,通过介绍物质的用途,化学原理的应用,化学在工农业生产、国防建设、现代化科学技术和日常生活中所起的重大作用,以及我国化学科学和化工生产在解放前后发展情况的事实的对比,对学生进行社会主义制度优越性和为实现四个现代化而学好化学的思想教育。通过有关科学家生平事迹的介绍,可对学生进行热爱科学、不畏艰难、攻克难关、坚韧不拔的思想品德教育。通过化学实验的教学,在教师以身示范的基础上,严格要求学生掌握科学实验方法的同时,对学生进行尊重事实、重视实践、实事求是的科学态度,整齐清洁、认真细致、一丝不苟、严肃认真、有条不紊的工作作风;遵守纪律、热爱劳动、勤俭节约、爱护公共财物等共产主义道德品质的教育。
在中学化学教学中,结合化学科学知识教学,对学生进行辩证唯物主义教育。培养学生的辩证唯物主义观点,是中学化学教学中体现科学性与思想性统一原则的一个重要方面。现将在中学化学教学中结合进行培养的一些重要观点,列举如下:
(一)关于“客观世界是物质的,是不依赖人类的意识而存在”的观点。例如,在讲到物质的组成——分子、原子、电子等时,要通过生动的事
例,如液体的蒸发,具有一定气味的气体的扩散等;或展示在电子显微镜下拍摄的由核蛋白分子组成的病毒照片,以及用场离子显微镜拍摄的反映钨原子排列的照片等,突出分子、原子存在的真实性。通过对电解质溶液的导电现象,以及对原电池、电解、电镀等事实的分析,使学生确信离子、电子的真实存在。
在讲到一些基本定律——质量守恒定律、元素周期律等时,一方面,应尽量做到由感性直观出发去揭示物质变化遵从这些规律;另方面讲解中要注意语言的科学准确性,这会起到潜移默化的效果,譬如决不可说人们创造了定律,而应说发现了定律,使学生明确它们都是客观存在的。同时,还要指出,至今还有许多客观事物未被发现,但将随着科学技术的发展会逐步认识
它们。
在讲授分子式、化学方程式等化学用语时,必须强调它们是代表客观存在着的化学事实,因此,决不能凭主观臆造。
(二)关于“自然界各种现象是不断变化、不断发展”的观点。
恩格斯指出:“整个自然界,由其最小部分到最大物体,由沙粒到太阳, 由原生物到人,都是处在永恒的产生和消灭过程中,处在毫不间断的流动中, 处在始终不停的运动和变化中”。
化学是研究物质及其变化的科学。在化学教学中,应当使学生深信世界上没有不变化的物质,也就是说没有绝对静止的物质。我们所说的静止,是相对静止;我们所说无变化是变化不显著,或处于平衡状态。
在中学化学教材中,到处都反映着物质不断变化、不断发展的科学事实。例如,在讲到物质的溶解、扩散、物质三态互变以及胶体的性质时,可以通过蔗糖的溶解、溴蒸气的扩散、胶体的布朗运动等实验现象,以及联系日常生活经验中水的三态互变等,向学生揭示物质的分子运动。讲到电离、电解时,可使学生观察高锰酸钾或氯化钴在水中的电离现象,以及氯化氢气体不能使干燥的蓝色石蕊试纸变红,而氯化氢的水溶液能使蓝色石蕊试纸变红的现象和水的电解等,向学生揭示离子运动。特别是当讲到化学平衡、电离平衡等时,更应揭示这只是正反应速度和逆反应速度相等时的动态平衡状态, 而并非化学反应的绝对终止。
再如讲到惰性气体时,应指出,过去曾经认为惰性气体绝对没有起化学变化的能力。这种“绝对”的形而上学观点阻碍了人们对惰性气体的研究长达六十多年之久,直到 1962 年以后,人们才发现惰性气体在一定条件下,也能跟其它物质发生化学反应。这个事实雄辩地证明,惰性气体也无一例外地存在着化学运动的属性。这个例子正好批判了形而上学观点在化学发展史中所起的阻碍作用。
结合种种化学运动的事实,要使学生明确“运动是物质存在的形式,是物质固有的属性”。没有运动的物质和没有物质的运动同样是不可思议的。物质世界就是在物质不断的运动变化中不断发展的。
(三)关于“自然界的变化是由量变到质变的过程”的观点。
恩格斯指出“化学可以称为研究物体在量的构成改变的影响下所发生的质变的科学。”
在化学上的量变,包括数量上的增减,如原子量、分子量、原子数目、以及温度、浓度、压力等的数量变化;和形状上的改变,如原子的大小,原子排列的方式以及空间的取向不同等。当这些因素的变化超过一定的量时, 会引起化学上的质变——物质的物理性质或化学性质的改变。[1]
在中学化学中,通过物质变化的教学,可以生动地揭示由量变到质变这一法则的普遍意义。
例如,在讲到氧气(O2)和臭氧(O3)二者性质的不同时,揭示这种同素异性体是由于组成分子中的原子数目和结合情况的不同(量变)而引起的质变。
在讲到水和过氧化氢、二氧化硫和三氧化硫、一氧化碳和二氧化碳等各由相同两种元素生成不同性质的化合物时,揭示这是由于相化合的原子数目的变化(量变)而引起的质变。
在讲到同系列有机化合物的性质差异时,揭示其间由于几种原子的数目
按一定比例增加(量变)而引起的质变。
在讲到浓硫酸与稀硫酸、浓硝酸与稀硝酸的性质不同时,揭示同一种物质因浓度不同(量变)而引起质变。
在讲到金刚石、石墨的不同性质时,要揭示这种同素异形体是由于晶格中原子排列的方式不同(量变)而引起的质变。
在讲到氢气和氧气的混和气体,在常温下不发生反应,而一经点燃就迅速发生反应时,要揭示这是由于温度的变化(量变)而引起的质变。
在讲述元素周期表中同周期元素由左到右性质递变和同族元素由上到下性质递变时,要揭示这是由于化学元素的核电荷数的变化(量变)而引起的质变等等。
(四)关于“自然界各个现象相互联系和相互制约”的观点。
通过教学要教育学生学会运用事物的相互联系和相互制约的观点去研究自然界的现象;在研究物质的变化时,一定要探求物质发生变化的原因和条件。例如,在讲到氢气和氧气完全化合而发生爆炸生成水的反应时,可指出: 氢气和氧气是发生反应的根据(内因),氢气与氧气的体积比为 2∶1,以及将混和气体点燃是发生反应的条件(外因)。只有这二者——发生反应的根据和条件均满足时,这个化学反应才得以顺利发生,否则就不能顺利发生。如上例若改为氢气和氦气的混和气体,虽按 2∶1 体积比混和并以火引之,却不能发生爆炸反应;或虽是氢气和氧气,并按 2∶1 的体积比混和,但保持常温而不点燃,则放置经年累月,仍不能发生爆炸反应。这样的分析,不但可以教育学生树立事物的相互联系和相互制约的观点;还使学生明确,要掌握一个化学反应,除应了解它的反应物和生成物外,还必须注意条件,从而使学生在书写化学方程式时,既重视正确书写反应物和生成物的化学式,又重视注明反应条件。
在中学化学教材中,氨的合成反应,是培养学生树立事物间相互联系和相互制约观点的一个典型反应,
N2+3H2
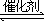 2NH3+热
2NH3+热
为了获得氨的最大的产率,必须逐个分析温度、压力、催化剂三者对合成氨的反应速度和化学平衡的影响,以寻求最适宜的生产条件。在实际生产过程中,还需考虑到设备材料和操作技术条件等因素的影响,以使所选择的生产条件有利于获得最大的经济效益。这样逐个分析温度、压力、催化剂的条件,而又综合考虑三者的影响,不仅对合成氨的生产条件讲得有趣、生动, 也有利于培养学生对具体事物应具体分析,以及事物间的相互联系和制约的辩证观点。
在元素及其化合物的教学中,教师运用事物间的相互联系和制约的观点进行复习总结,不仅有利于学生认识事物间的相互联系的客观规律,还可使学生获得系统的知识,并使知识得到深化,有利于学生牢固的掌握。如在碳元素及其化合物的教学之后,以各物质及其变化的内在联系的规律来进行总结复习,可列出以下的各物质相互变化的关系图进行复习总结。
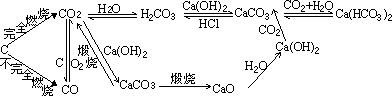
(五)关于“事物的矛盾法则”即“对立统一的法则”的观点。
辩证唯物主义原理指出,事物发展的根本原因,不是在事物的外部而是在事物的内部,在于事物内部的矛盾性。事物的矛盾法则,即对立统一的法则。在化学中,对立统一的法则是普遍存在着的。例如,分子本身就是吸引和排斥矛盾双方的对立统一体,另如氧化与还原、化合与分解、中和与水解、溶解与沉淀、弱电解质在溶液中的电离与结合,以及平衡与不平衡等等,这些变化的实质都是矛盾斗争的对立统一过程。
在中学化学教学中,对学生进行对立统一法则的观点的教育时,应抓住典型教材明确以下观点:
第一,矛盾双方的斗争是绝对的。统一是相对的,例如,化学平衡,与其他一切平衡一样都只是相对的、暂时的和有条件的。而不平衡则是绝对的。化学平衡是一种动态平衡。
第二,矛盾着的双方互相斗争的结果,无不在一定条件下互相转化。因此,在一定条件下达到化学平衡后,当条件改变时,平衡就要被破坏而发生移动,在新的条件下重又达到新的暂时的平衡。
第三、矛盾着的双方互为存在的条件。例如,没有不同元素的化合,就没有化合物的分解。在氧化还原反应中,一物质被氧化,另一物质就必然被还原,氧化和还原这两个相反过程同时存在于氧化还原反应这一矛盾的统一体中。
第四,事物的性质和变化,主要是由取得支配地位的矛盾的主要方面所规定的。例如在讲 HCl+NaOH=NaCl+H2O 的中和反应时,可指出溶液中存在着以下过程:
 HCL
H++Cl-
HCL
H++Cl-
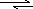 NaOH
Na++OH-
NaOH
Na++OH-
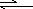 Na++Cl-
NaCl
Na++Cl-
NaCl
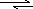 H++OH-
H2O
H++OH-
H2O
以上四对矛盾中,只有 H+和 OH-结合的产物 H2O 是难电离的物质。因此, 酸、碱中和反应的主要矛盾是水的电离平衡,其中矛盾的主要方面是酸中的H+与碱中的 OH-相互结合生成难电离的水的过程,这就是中和反应的实质。
