1. 热分解反应:
============
 少数热力学上不稳定的重金属氧化物、硫化物可用热分解法制取2HgS+3O2
2HgO+2SO2
少数热力学上不稳定的重金属氧化物、硫化物可用热分解法制取2HgS+3O2
2HgO+2SO2
 2HgO
2Hg+O2
2HgO
2Hg+O2
 2Ag2O
4Ag+O2
2Ag2O
4Ag+O2
 由上可知,提取金属的反应主要有两类:一是水溶液中进行的还原反应,
可以依据ϕ
选择合适的还原剂;另一是固相热还原反应和热分解反应,它们可以根据艾林汉(Eillingham)图来判断反应的方向和趋势的大小。
由上可知,提取金属的反应主要有两类:一是水溶液中进行的还原反应,
可以依据ϕ
选择合适的还原剂;另一是固相热还原反应和热分解反应,它们可以根据艾林汉(Eillingham)图来判断反应的方向和趋势的大小。
艾林汉(Eillingham)图简介
 艾林汉在
1944
年首先将氧化物的标准生成自由能对温度作图,后又对硫化物、氯化物、氟化物等作类似图,这种△rG
—T
关系图称为艾林汉图。用这种图可知任何一类化合物中哪些金属化合物稳定,可比较直观地从图上判断反能否进行,以及该过程倾向的大小。故在冶金上有重要应用。
艾林汉在
1944
年首先将氧化物的标准生成自由能对温度作图,后又对硫化物、氯化物、氟化物等作类似图,这种△rG
—T
关系图称为艾林汉图。用这种图可知任何一类化合物中哪些金属化合物稳定,可比较直观地从图上判断反能否进行,以及该过程倾向的大小。故在冶金上有重要应用。
图 11—6 是用消耗 ImolO2 生成氧化物过程的自由能变化对温度作图的。
根据





 △rG
=△rH -T△rS
△rG
=△rH -T△rS






 的关系,只要△rS
不等于零,则△rG 将随温度的改变而改变。假如△rH 和 T△rS 为定值,则△rG
对绝对温度作图便得一直线,直线的斜率等于熵变。在 0K 时,△rG =△rH
,此时直线与纵座标的截距即为△rH
近似值,只要反应物或生成物不发生相变(熔化、气化相转变)△rG 对 T
作图都是直线。因为如有相变,必定会有熵变,由于熵变是直线的斜率。所以当发生相变时,直线斜率将会改变。
的关系,只要△rS
不等于零,则△rG 将随温度的改变而改变。假如△rH 和 T△rS 为定值,则△rG
对绝对温度作图便得一直线,直线的斜率等于熵变。在 0K 时,△rG =△rH
,此时直线与纵座标的截距即为△rH
近似值,只要反应物或生成物不发生相变(熔化、气化相转变)△rG 对 T
作图都是直线。因为如有相变,必定会有熵变,由于熵变是直线的斜率。所以当发生相变时,直线斜率将会改变。

 图
11—6 由氧化物的△rG —T 图可以得到一些金属还原反应的规律:
1.一个反应要能进行,其△rG 必须为负值,从图可看出,凡△rG 为
图
11—6 由氧化物的△rG —T 图可以得到一些金属还原反应的规律:
1.一个反应要能进行,其△rG 必须为负值,从图可看出,凡△rG 为

 负值区域内的金属都能自动被氧气氧化,凡在这个区域以上的金属则不能,
负值区域内的金属都能自动被氧气氧化,凡在这个区域以上的金属则不能,

 例如银。某些金属随温度的升高,△rG
负值减小,当直线与△rG =O 的水平线相交超过这一水平线时,表明△rG
≥O,这意味着超过这个反应温度时,氧化不能自发进行。在△rG ≥O
的区域内氧化物是不稳定的,会自发分解。例如反应:
例如银。某些金属随温度的升高,△rG
负值减小,当直线与△rG =O 的水平线相交超过这一水平线时,表明△rG
≥O,这意味着超过这个反应温度时,氧化不能自发进行。在△rG ≥O
的区域内氧化物是不稳定的,会自发分解。例如反应:
2HgO→2Hg+O2
 在
773K 以上就可以分解得到金属汞。
在
773K 以上就可以分解得到金属汞。





 氧化物的稳定性和其△rG
值大小直接有关,稳定性差的氧化物△ rG 负值小,△rG —T
直线位于图上方,例如 Ag2O、HgO。稳定性高的氧化物△rG 负值大,△rG —T
直线位于图下方,如 MgO、CaO。在△rG —T
图中,一种氧化物能被位于其下面的那些金属所还原,因为这个反应的△rG
氧化物的稳定性和其△rG
值大小直接有关,稳定性差的氧化物△ rG 负值小,△rG —T
直线位于图上方,例如 Ag2O、HgO。稳定性高的氧化物△rG 负值大,△rG —T
直线位于图下方,如 MgO、CaO。在△rG —T
图中,一种氧化物能被位于其下面的那些金属所还原,因为这个反应的△rG
<0,例如在 1073K 时,Cr2O3 能被铝还原,而 Al2O3 就不能被铬还原。
- 图中 C+O2→CO2 的直线几乎是水平的,即其斜率≈0,这个反应实际上没有熵变,因反应开始和终了气体分子数不变,固体熵变可以忽略。
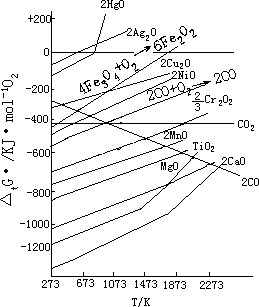
 图
11-6 氧化物的△rG -T 图
图
11-6 氧化物的△rG -T 图

 反应
2C(s)+O2(g)→2CO(g)的直线向下倾斜,即具有负的斜率, 这是因为 1
体积的 O2 生成了 2 体积的
CO,气体分子数增加,熵增加很大,故温度升高,△rG 变得更负。
反应
2C(s)+O2(g)→2CO(g)的直线向下倾斜,即具有负的斜率, 这是因为 1
体积的 O2 生成了 2 体积的
CO,气体分子数增加,熵增加很大,故温度升高,△rG 变得更负。
反应 2CO+O2→2CO2 的直线因熵变为负值,所以温度越高,反应的△rG 增大,直线从左向右向上倾斜。三直线交于 983K。高于此温度,2C+O2→2CO 的反应倾向大,低于此温度,2CO+O2→2CO2 的反应倾向更大。

 生成
CO 的直线向下倾斜对于火法冶金有很大实际意义,这使得几乎所有金属的△rG 一
T 直线在高温下都能与 C—CO
直线相交。这表明许多金属氧化物在高温下能被炭还原,使炭成为一种优良的还原剂。但实际上由于高温时设备困难和易生成碳化物,使它的应用受到限制,最后应指出,用△rG
判断反应方向只考虑平衡态,并不涉及动力学问题,实际上选择还原剂时,
需对问题作全面、具体的分析,才能得出正确的结论。
生成
CO 的直线向下倾斜对于火法冶金有很大实际意义,这使得几乎所有金属的△rG 一
T 直线在高温下都能与 C—CO
直线相交。这表明许多金属氧化物在高温下能被炭还原,使炭成为一种优良的还原剂。但实际上由于高温时设备困难和易生成碳化物,使它的应用受到限制,最后应指出,用△rG
判断反应方向只考虑平衡态,并不涉及动力学问题,实际上选择还原剂时,
需对问题作全面、具体的分析,才能得出正确的结论。
