二、颜色与立体化学环境有关吗?
颜色与立体化学环境密切相关,人们很早就发现 Co(Ⅱ)化合物的颜色分为两大类:红色的基本上是八面体配合物,蓝色的基本上是四面体配合物,
 当向
CoCl2 水溶液分别加入浓 HCl、浓
NaOH、NH4SCN,溶液均由红色变为蓝色,即由八面体[Co(H2O)6]2+变为四面体离子[CoL4]2-离子(L=Cl-,OH-
, SCN-)水溶液中存在平衡:
当向
CoCl2 水溶液分别加入浓 HCl、浓
NaOH、NH4SCN,溶液均由红色变为蓝色,即由八面体[Co(H2O)6]2+变为四面体离子[CoL4]2-离子(L=Cl-,OH-
, SCN-)水溶液中存在平衡:
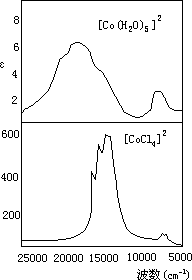
图 2 [Co(H2O)6]2-和[CoCl4]2-的电子光谱
在 Co(Ⅱ)晶体中也有类似情况,如由四个氧原子四面体配位的钴蓝
(Mg,Co)Al2O4 尖晶石结构和正硅酸盐蓝(Zn,Co)2SiO4(硅锌石结构) 都是蓝色的,而 CoF2(金红色结构)八面体配位为红色。
Co(Ⅱ)八面体化合物和四面体化合物颜色不同在于它们晶体场分裂能不同,根据计算△四面体=4/9△八面体即 d 电子在四面体场中跃迁所需能量比八面体场小。比较[(Co)(H2O)6]2+ 和[(CoCl4]2-的电子光谱就可看出它们
有明显的差别(图 2),红色八面体配合物在近可见光区 20000cm-1 有弱多重吸收带。另一吸收带在 8000cm-1 附近,四面体配合物是深蓝色,一般见到两个吸收带 15000cm-1 和 5800cm-1。
类似这种情况在 Cu(Ⅱ)化学中也存在,Cu(Ⅱ)氯化物颜色变化范围从严重畸变的四面体配位的 Cs2CuCl4 的柠檬黄色经过深红色的 CsCuCl3 到棕色 CuCl2,后两者晶体为畸变八面体配位,而 Cu(Ⅱ)的水合盐却与这些不同为蓝色,CuCl2,2H2O 晶体和 K2CuCl4,2H2O 虽也都是畸变八面体配位,但其中金属原子与 4 个 Cl-离子和 2 个 H2O 分子键合。由此可见,考虑一个物质的颜色时应注意与它们的立体化学环境联系起来,切忌孤立地讨论某种金属离子的颜色而引起误解。
