二、“假说——实验·推理”教学法的课堂模式及其应用
一般教材上的知识大多包含不到环节:①提出本节课要解决哪些问题。
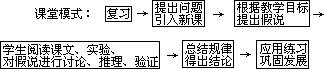 ②用什么理论或定理来解决这些问题。③得出什么样的结论或规律。④该问题的应用。这些环节在学习新课时,多数学生掌握不了。闻此,教师应根据本节课的教学目标和内容,向学生明确提出的以上的教学环节。具体的程序如下
②用什么理论或定理来解决这些问题。③得出什么样的结论或规律。④该问题的应用。这些环节在学习新课时,多数学生掌握不了。闻此,教师应根据本节课的教学目标和内容,向学生明确提出的以上的教学环节。具体的程序如下
(一)在新得教学中的应用
例如:在学习 O2 在制备时,教师提出如下问题。(1)用加热 KClO3 制取O2 时为什么要加 MnO2?不加分解不分解?(2)MnO2 在这个反应中起什么作用?它的质量和化学性质在反应前后是否发生变化?这两个问题提出后,学生会积极开动脑筋进行思考,自然地进入问题的情景,使他们的注意力迅速集中到问题上。
教师在课前认真设计,提出假说。如( 1)加热 KClO3 时不加 MnO2 不会
产生 O2;(2)加入 MnO2 后,加热 KClO3 产生 O2 的量增加;(3)加入 MnO2 后,KClO3 可以较低的温度下迅速分解。
提出假说之后,要求学生慎重地选择一种假说,并让他们充分运用已有的知识和经验来论证自己所持的假说,以培养学生的判断能力,逻辑推理能力和语言表达能力,最后用实验来验证。
由实质的结果总结出如下的规律:加热 MnO2 不产生 O2,但它能使 KClO3 在较低温度下迅速产生 O2,其本身的质量和化学性质并没有改变。进而引导学生总结出:具有上述性质的物质叫做催化剂。最后用此概念(规律)来解题:“加热 50 克 KClO3 和 MnO3 的混合物来制取 O3,加热前 MnO2 占 20%,当加热此混合物至 MnO2 占固体混合物 25%时产生 O2 的质量为多少克?”
再如:对“乙醇分子结构”的认识。首先提出“乙醇分子具有怎样的结构”的问题,然后根据乙醇的化学式和碳、氢、氧的化合物写出乙醇分子的两种可能结构式(提出假说):
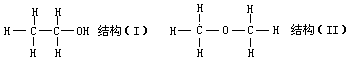
如果是结构(Ⅰ)那么 1mol 乙醇能产生 0.5mol 或 2.5molH2;如果是结构(Ⅱ)那么 1mol 乙醇能产生 3molH2。测定和记录一定量的乙醇跟钠反应所产生的 H2 的体积(实验验证)。经计算,1mol 乙醇大约能产生 0.5molH2。据此可以得出结论:乙醇分子的结构是结构(Ⅰ)。
(二)在复习课习题教学中的应用
有一色固体粉末混合物,其中可能含有适量的 CaCO3、炭粉、CuO、 Fe2O3 中的一种或几种。现作如下实验。(1)取混合物少量,高温灼烧后,产生一种能使石灰水变浑浊的气体。(2)把足量的稀盐酸滴入上面灼烧后的残存固体物质中,固体全部溶解,同时产生一种最轻的气体。
回答:①混合物中一定不含有的物质是 。②混合物中一定含有的物质是 。③混合物中可能含有的物质是 ,为了证明这种物质是否存在,你认为可采用的方法和依据的化学原理是什么?
- 提出问题:
-
把以上四种物质单独灼烧或相互混合灼烧,哪些能产生 CO2?
-
投入稀盐酸能产生 H2 的物质可能是什么?
问题提出后,教师有意识地组织学生就该问题有关知识进行回顾、复习, 以便为解决问题做好准备。
 提出假说:
提出假说:
 上述问题(1)教师引导学生得出以下四种假说:①可能是
C:C+O2 CO2
上述问题(1)教师引导学生得出以下四种假说:①可能是
C:C+O2 CO2

 ②可能是
CaCO3 :CaCO3 CaO+CO2 ↑③可能是 C 和 Fe2O3 的混合物: C+2Fe2O3
4Fe+3CO2↑④可能是 C 和 CuO 的混合物:C+2CuO 2Cu+CO2
②可能是
CaCO3 :CaCO3 CaO+CO2 ↑③可能是 C 和 Fe2O3 的混合物: C+2Fe2O3
4Fe+3CO2↑④可能是 C 和 CuO 的混合物:C+2CuO 2Cu+CO2
↑
- 对假设进行推理讨论:
引导学生根据题目的第二个已知条件“残存固体全部溶解(于盐酸), 同时产生一种最轻的气体(即 H2)”来判断选择一种假说,并说出这种假设说的理论依据。
- 得出结论:混合物中一定含有 C、Fe2O3,一定没有 CuO,可能会有 CaCO3。
