二、培养学生对问题的对立、比较的思维能力
比较是确定现实对象和现象的异同的一种思维过程,将不同对象进行对比,确定其异同,通过比较,抓住事物的本质,突出矛盾的特殊性。
氧化还原反应是一类重要的化学反应。只有让学生理解氧化还原反应的概念,才能掌握许多重要元素及其化合物反应的实质。氧化还原反应是一对矛盾,既对立又统一于同一反应中,伴同反应,相互依存。教学中首先必须使以下知识到位:
实质 - 失去电子(或共用电子对偏移)的反应
氧化
- 反应
特征 - 化合价升高
实质 - 得到电子(或共用电子对偏近)的反应
还原
特征 - 化合价降低
还原剂:含有可失电子的元素的物质,使对方还原的物质。
- 物质
氧化剂:含有可得电子的元素的物质,使对方氧化的物质。
氧化性- 夺取电子的性质- 氧化剂具有氧化性
- 性质 还原性- 失去电子的性质- 还原剂具有还原性
氧化产物- 还原剂失电子后的产生
- 产物
还原产物- 氧化剂得电子后的产物
上述关于氧化还原的四个对立关系就是氧化还原反应的概念术语之间的逻辑关系。
教学过程是一个以“教”到“学”的过程,上述知识结构切实到位后, 必能转化为学生学习氧化还原反应的能力,有了能力,就能运用知识,就可确定解题的基本思路。
在弄清上述知识结构之后,应不失时机地把思维能力往纵深发展,适时地提出:
- 原子、离子和氧化、还原的关系

- 根据反应式判断氧化性、还原性的强弱:
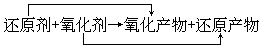
氧化能力:氧化剂>氧化产物,还原能力:还原剂>还原产物。
