磷酸盐
磷酸的盐类。皆为固体,溶解性按正盐、一氢盐、二氢盐依次渐增。其钠或钾盐的水解,其二氢盐呈微酸性,一氢盐微碱性,正盐碱性,
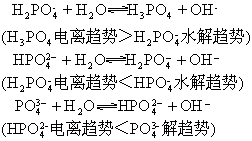
正盐遇酸视酸量不同可转化为磷酸、二氢盐或一氢盐;一氢盐与酸亦可转化为磷酸或二氢盐;二氢盐与强酸则有磷酸生成。磷酸酸
式盐与不同量碱可转化为正盐或含氢更少的酸式盐。可知PO3- 只存于碱性
环境,而HPO2- 和H PO- 不能与强酸或强碱大量共存。由磷矿石或磷酸
4 2 4
加工可制得磷酸盐。磷酸与足量碱生成正盐。磷酸与碱中 OH? 的物质的量比为 1:2 时生成一氢盐;为 1:1 时生成二氢盐。磷酸的正盐与酸反应生成不同磷化合物,主要代表物为 Ca3(PO4)2。如它与硫酸反应可生成 Ca(H2PO4)2, 是制高效磷肥重过磷酸钙的主反应。Ca3(PO4)2 与 H2SO4 反应的量的关系(设na 为 H2SO4 的物质的量,nb 为 Ca3(PO4)2 物质的量)为:na/nb≤2 生成 CaHPO4、na/nb<2 生成 CaHPO4 与 Ca(H2PO4)2 混合物、na/nb=2 生成 Ca(H2PO4)2、na/nb
<3 生成 Ca(H2PO4)2 与 H3PO4 的混合物,na/nb≥3 生成 H3PO4。上述反应的另一生成物皆为 CaSO4。磷酸盐主要用做化肥,如过磷酸钙、重过磷酸钙、磷矿粉等单一磷肥和磷酸铵类复合磷肥以及喷施的磷酸二氢钾类磷肥;Na3PO4 是常用的洗涤剂和锅炉防垢剂;其它用途如二氢盐用于发酵粉和用磷矿与焦炭、石英于高温制取白磷等。
