离子方程式
用实际参加反应的离子符号表示离子反应的式子。它不仅表示一定物质间的某个反应,而且表示了所有同一类型的离子反应。
书写离子方程式的基本步骤为:①写出有关反应的化学方程式。②可溶性的强电解质(强酸、强碱、可溶性盐)用离子符号表示,其它物质仍用分子式表示。微溶的强电解质应看其是否主要以自由离子形式存在,例如,石灰水中的 Ca(OH)2 写离子符号,石灰乳中的 Ca(OH)2 用分子式表示。③删去两边未参加反应的离子。④检查式子两边的各种原子的个数及电荷数是否相等。
各种类型的离子方程式可按下列方法书写:①络合反应、盐类的水解反应应直接写离子方程式。例如,氯化铁溶液跟硫氰化钾溶液反应:
 Fe3++SCN-
[Fe(SCN]2+
Fe3++SCN-
[Fe(SCN]2+
碳酸钠水解:
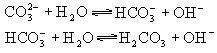
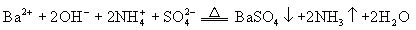 ②简单的复分解反应可直接写出离子方程式。注意:当反应物一边或生成物一边有多种物质需用分子式表示时,应当写全,不可遗漏。例如,氢氧化
钡 与 硫 酸 铵 溶 液 共 热 :
②简单的复分解反应可直接写出离子方程式。注意:当反应物一边或生成物一边有多种物质需用分子式表示时,应当写全,不可遗漏。例如,氢氧化
钡 与 硫 酸 铵 溶 液 共 热 :
可溶性酸式盐跟强碱的反应比较复杂,应按基本步骤书写,否则易出错误。例如,磷酸二氢钙溶液与足量烧碱溶液反应,以下离子方程式是错误的:
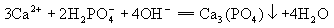
应 先 写 出 化 学 方 程 式 : 3Ca(H2PO4)2+12NaOH=Ca3(PO4)2↓+12H2O+4Na3PO4
再删去 Na+:
3Ca 2+ + 6H PO− + 12OH − = Ca ( PO ) ↓ +12H O + 4PO3−
2 4 3 4 2 2 4
③氧化还原类型的离子反应应按基本步骤书写,否则会出现多种错误。例如, 铁跟氯化铁溶液反应,以下写法是错误的(两边电荷不等):
Fe+Fe3+=2Fe2+
应先写出化学方程式: 再删去未反应的 Cl-:
Fe+2FeCl3=3PeCl2 Fe+2Fe3+=3Fe2+
再如,氯气跟溴化亚铁溶液的反应,以下写法均不正确:
2Fe2++Cl2=2Fe3++2Cl-
2Br-+Cl2=Br2+2Cl-
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
只有先写出化学方程式才能避免以上错误。正确书写方法为: 化学方程式:
2FeBr2+3Cl2=2FeCl3+2Br2
离子方程式:
2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2
