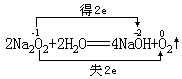氧化还原反应中电子转移方向与数目的判断及表示
在氧化还原反应中,氧化剂得电子,表现为所含元素化合价降低;还原剂失电子,表现为所含元素化合价升高;得失电子数与化合价升降数相等。因此,电子转移的方向和数目可通过元素化合价的变化判断。在反应中,某元素电子得失总数等于该元素一个原子化合价升降数乘以方程式系数。主要表示方法有两种:①表示同一元素反应前后电子转移情况时,分别将氧化剂与其产物、还原剂与其产物中相应的变价元素用直线连接起来,箭头从反应物指向产物,线上标出得失电子总数,称为“双线桥法”。②表示氧化剂和还原剂之间不同元素的电子转移情况时,将氧化剂中降价元素与还原剂中升价元素用直线连接起来,箭头从还原剂指向氧化剂,线上标出电子转移总数, 称为“单线桥法”。例如,铁与氯气的反应。双线桥法:
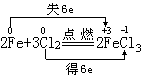
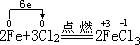 单线桥法:
单线桥法:
通常情况用单线桥法表示比较简单,且易判断出氧化剂和还原剂(箭头所指为氧化剂)。在同种元素发生自身氧化还原反应时,用双线桥法表示比较明确, 例如,过氧化钠跟水反应。