实验方案的设计
实验方案一般包括实验路线的优选;仪器和药剂的选择;实验装置的组合;操作程序的编排及条件的控制;数据的测量等。例如:
1.用测量一定量电石跟水反应产生的乙炔的体积的实验方法,测定电石中 CaC2 的百分含量,设计实验装置并指出操作程序和方法。
可用烧瓶配分液漏斗作乙炔发生装置,收集乙炔并排出水可用广口瓶配双孔胶塞组装,排出水的体积用量筒测量。组合装置如下图:
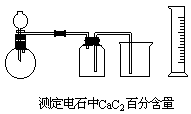
操作程序是:(1)在广口瓶内加水至满,(2)检查气密性(设法使广口瓶和烧杯间的导管里充满水),(3)向烧瓶里加入一定量的电石(由广口瓶的容积计算而得。设容积是 500 毫升,则电石用量以 1.1~1.2 克为宜)。(4)从分液漏斗缓缓滴水至不再发生气体为止,(5)待烧瓶恢复常温后(控制条件),测量排出水的体积,记下数据并换算成标准状况,(6)根据有关数据计算 CaC2 百分率。 2.工业水煤气中含 CO、H2 及少量水蒸气和 CO2,为了证实水煤气中含 CO
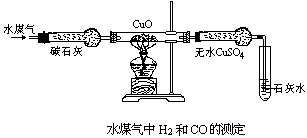 和
H2,设计简易组合实验装置,注明所用试剂并指明有关现象和结论。整体思路是:跟
CuO(加热)反应后有水生成,证明含 H2;有 CO2 生成,证明含
CO。检验生成水,用无水 CuSO4;检验生成 CO2
用澄清石灰水。关键的问题是水煤气跟 CuO
反应之前须先除去混合气体中的水蒸气和 CO2,否则,得不出可靠的结论。除 CO2
可用碱溶液,除水蒸气可用浓硫酸,但必须先除 CO2
后除水蒸气。如用碱石灰,则可同时除去置更简便。根据以上思路,设计装置如下:
和
H2,设计简易组合实验装置,注明所用试剂并指明有关现象和结论。整体思路是:跟
CuO(加热)反应后有水生成,证明含 H2;有 CO2 生成,证明含
CO。检验生成水,用无水 CuSO4;检验生成 CO2
用澄清石灰水。关键的问题是水煤气跟 CuO
反应之前须先除去混合气体中的水蒸气和 CO2,否则,得不出可靠的结论。除 CO2
可用碱溶液,除水蒸气可用浓硫酸,但必须先除 CO2
后除水蒸气。如用碱石灰,则可同时除去置更简便。根据以上思路,设计装置如下:
无水硫酸铜由白变蓝,可证明有水生成,说明原混合气中含 H2,石灰水变浑浊,证明生成物有 CO2,说明原混合气中含 CO。
