浅探初中化学中的一般与特殊 山东省菏泽市马村集乡中学 刘振方
客观事物是复杂的,看问题要从各方面看,而不能只从单方面去看。任何一门科学知识都是有规律可寻的。在初中化学中存在着许多规律性的知识,凡规律性的知识,既有普遍性又有特殊性,努力探讨这些普遍性和特殊性,既是教师全面掌握教材、深刻理解教材,并贯彻于实际教学的需要,也是学生运用课本知识提高分析问题和解决问题的能力,迎接各种测试,提高教学成绩的需要。
现根据笔者在多年的教学实践中,向学生揭示的一般与特殊的情况,归纳整理出来,略述己见,以供同仁们酌商,旨在起到抛砖引玉的作用。由于笔者学识浅薄,经验匮乏,文中不当及谬误之处,在所难免,恭请各位专家学者及同行斧正。
-
原子核一般是由质子和中子组成的,但并非任何元素的原子核都是由质子和中子组成的,如,氢原子核只有质子而无中子。
-
在溶液中,一般习惯上把液态物质称为溶剂,非液态物质称为溶质, 但根据溶液的概念,清新的空气也可以称之为溶液,而这种溶液中的溶质和溶剂均为气体。
-
含氧酸一般是根据其组成时氢氧两种元素以外的另一种元素而命名的。硝酸按命名规则应该叫氮酸,但通常情况下叫硝酸,这是因为硝酸最早是用硝石制造的。
-
氧气在通常情况下,一般是一种无色无味的气体,但在 1 个标准大气压下,氧气在-183℃时变为淡蓝色的液体,在-218℃时变成雪花状的淡蓝色固体。
-
自然界里的含碳物质一般是一些复杂的物质,但金刚石、石墨等少数几种物质是由碳一种成分组成的简单物质。
-
稀有气体元素的原子,其最外电子层上一般是 8 个电子,但氦原子只
有一个电子层,且该层上只有 2 个电子。
-
化学上一般把含碳的化合物叫做有机物,不含碳的化合物叫做无机物,但 CO、CO2、H2CO3 等少数简单的化合物,由于结构和性质跟无机物根相近,所以习惯上把它们称为无机物。
-
非金属单质一般不导电,没有金属光泽,但非金属单质石墨既能导电又有金属光泽。
-
金属单质在常温下一般是固体,但金属单质汞是液体。
-
氯化物一般都能溶于水,但 AgCl、HgCl 不溶于水。
-
书写化合物的化学式时,元素的排列顺序一般是正价前负价后,但CH4、C2H2、NH3 却是负价前正价后。
-
由两种元素组成的化合物的名称,一般是由右向左读作“某化某”, 但 CH4、C2H2、NH3 却不能由右向左读作“某化某”,而只能分别读作甲烷、乙炔、氨气。
-
根在一般情况下是由两个以上的原子结合而成的原子团,但盐酸根却只有一个氯原子组成。
-
酸一般是纯净物,但盐酸却是混合物,因为盐酸是氯化氢气体的水溶液。
-
原子团一般在许多化学反应里作为整体,好像一个原子一样,反应前
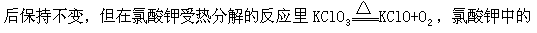
氯酸根(ClO3)就发生了变化。
-
书写化合物的化学式,一般可用“双交叉法”书写(即符号排列由名称中元素交叉得到,角码由元素化合价交叉得到)。但 Fe3O4 例外,因为 Fe3O4 中的三个铁原子中有 2 个铁原子显+3 价,1 个铁原子显+2 价,各元素化合价的代数和仍为零,与化合价法则并不矛盾。
-
根据氧分物性质的不同,氧化物一般可分为酸性氧化物和碱性氧化物,但氧化铝和氧化锌既不是酸性氧化物也不是碱性氧化物,而是两性氧化物。
-
大多数固体物质的溶解度随温度的升高而增大,少数固体物质的溶解度受温度的影响不大,还有极少数固体物质的溶解度随温度的升高而减少, 如氢氧化钙。
-
大多数金属氧化物一般是碱性的,但 CrO3、Mn2O7 是酸性的,Al2O3、ZnO 是两性氧化物。
-
一种元素一般只能组成一种单质,但碳可组成金钢石和石墨、磷可组
成红磷和白磷两种不同的单质。
-
燃烧一般有氧气参加,但燃烧并非一定要有氧气参加,例如,氢气和钠可分别在氯气中燃烧,镁可在二氧化碳中燃烧。
-
用水稀释溶液时,一般可把水倒入溶液中,但用水稀释浓硫酸时,却必须把浓硫酸倒入水中,并且要用玻璃棒不断地搅拌,以免形成暴沸,造成事故。
-
爆炸一般是由化学反应引起的,但爆炸并非都是化学反应,有些爆炸仅仅是一个物理过程,如蒸气锅炉的爆炸。
-
一个化学式一般只表示一种物质,但 HCl 这个化学式既可以表示盐酸又可以表示氯化氢。
-
化合物中某种元素的化合价一般只有一种,但在 NH4NO3 中,氮元素的化合价既显-3 价又显+5 价。
-
向澄清的石灰水中通入 CO2,一般会产生白色沉淀,但当通入过量的
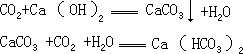 CO2
时,白色沉淀反而会消失,这是因为:
CO2
时,白色沉淀反而会消失,这是因为:
-
给物质加热时,酒精灯一般是先点后撤,但当用 H2、CO 还原 Cuo 时, 酒精灯却是后点先撤。
-
化学肥料一般只含一种营养元素,但(NH4)3PO4、KH2PO4 等却含有两
种营养元素。
-
化学肥料一般易溶于水,但钙镁磷、磷矿粉却难溶于水。
-
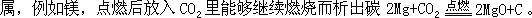 在一般情况下,CO2
在一般情况下,CO2既不能自燃也不助燃。但对某些活动性大的金
-
气体单质一般是由分子构成的,而且是双原子分子,但稀有气体单质却是由原子直接构成的。
-
酸性氧化物一般能直接跟水反应生成酸,但 SiO2 例外,因为 SiO2 不溶于水。
-
大多数碱性氧化物一般不能跟水后应生成碱,但有些碱性氧化物却能
直接跟水反应生成碱。如 K2O、Na2O、BaO 等。34.酸一般都能溶于水,但硅酸不溶于水。
- 盐跟金属的反应一般遵循金属活动性顺序的规律,即在金属活动性顺
序表里,只有排在前面的金属,才能把排在后面的金属从它们的盐溶液里置换出来,但某些很活泼的金属,如钾钠等,它们与排在其后面的金属盐溶液反应,一般不会有金属被置换出来,例如:
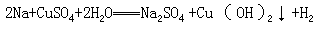
- 金属和酸的反应一般遵循金属活动性顺序的规律,即排在氢前面的金属能置换出酸中的氢,排在氢后面的金属不能置换出酸中的氢。但当活泼金属与氧化性很强的硝酸、浓硫酸等反应时,就没有氢气放出,例如:
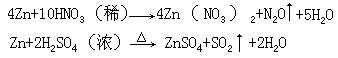
-
化学元素的读音,一般都是按偏旁字发音的,但也有不少例外,如氧读作“养”,钠读作“纳”,“溴”读作“秀”。有些元素名称,常被读错,
例如:铬应读作“各”,现常读作“洛”,氙本应该“仙”,现常误读为“山” 等。
-
一般从宏观组成上给各类物质下定义,但有时也从微观组成上给物质下定义,如金属离子和酸根离子组成的化合物叫做盐等。
-
一般来说,绝大多数金属都可与氧反应,但 Ag、Pt、Au 除外。
-
不溶性碱一般在加热条件下,能脱水生成碱性氧化物,但 Al(OH)3 、Zn(OH)2
在加热的条件下生成两性氧化物。
-
一般来说,非金属绝大多数都能直接和氧反应,但 F2、Cl2、Br2、I2 除外。
-
在金属元素和非金属元素形成的化合物中,由于金属元素很少有变
 价,所以在物质名称中一般不表示出数了,但对于
Fe3O4
却必须表示出数字。43.大多数固体物质两种溶液相互转化的条件一般如下:饱和溶液
价,所以在物质名称中一般不表示出数了,但对于
Fe3O4
却必须表示出数字。43.大多数固体物质两种溶液相互转化的条件一般如下:饱和溶液
的升高而减少的固体物质例外,如 Ca(OH)2。
-
酸一般为液体,但也有呈固态的,如 H3PO4、H2SiO3。
-
固体单质的化学式一般只用元素符号表示,但碘用 I2 表示。
-
一般情况下,可根据元素的化合价书写化合物的化学式,也可以根据化合物的化学式判断元素的化合价,但
Fe3O4 例外,实际上 Fe3O4 是个复杂的化合物,其组成可以看作为 Fe2O3·Feo,因此在 Fe3O4 分子中,有两个铁原子显+3 价,一个铁原子显+2 价,由此可知,Fe3O4 是个特殊的物质。
-
含变价金属的化合物,一般不显白色,但 CuSO4 却显白色。
-
水一般是无色、透明的液体,但水深的时候却显浅绿色,再深的又显蓝绿色,更深的会显深蓝色甚至显黑色。这是因为不同深度的水对光的吸收和反射的情况不同决定的。
-
现在我国通用的化学元素汉语名称里,凡是金属,一般都写作“金”
旁,但例外的是一种金属汞,因为它在常温下是液体(“水”代表液态)。
-
二氧化硫通常情况下一般是无色气体,但干冰(固态的二氧化碳)却是一种半透明的白色固体。
-
测定溶液的酸碱度,一般选用 pH
试纸,但是当要精确测定溶液的酸碱度时却要用 pH 计。
-
在用天平测量物体的质量时,物体的质量一般等于砝码的质量和游码的质量之和,但当物体和砝码的质量放翻时,则物体的质量应为砝码的质量与游码的质量之差。
-
两种液体相互溶解时,一般把量多的一种叫做溶剂,量少的一种叫做溶质,但溶质和溶剂是相对而言的,例如,酒精和水互相溶解时,一般来说酒精是溶质,水是溶剂;如果把少量水溶解在酒精里,就可以把水作为溶质,
酒精作为溶剂。
-
一般在常温下,碳的化学性质不活泼,但随着温度的升高,碳的活动性大大增强。在高温下,碳能跟多种物质起反应。例如碳能在高温下夺取氧
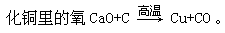
-
在化合物里,金属元素一般显正价,非金属元素一般显负价。但在非金属氧化合物里,氧显负价,另一非金属元素显正价。氧和氢在它们各自的化合物里,氧一般显-2。氢一般显+1
价。
-
有机物一般难溶于水,但 C2H5OH、CH3OH、CH3COOH 等却易溶于水。
-
酸一般都能受热分解生成对应的酸酐和水,但醋酸硝酸例外。
-
带正电荷的离子一般是金属离子,但带正电荷的离子不一定都是金属离子,例如
H+、NH+4。
-
溶液一般为液体,但并不是所有的溶液都是液体,例如,空气是一种气体溶液,合金、玻璃是一种固体溶液。
-
碳酸盐大多数一般不溶于水,但钾、钠、铵的碳酸盐能溶于水。
-
化学题目中的信息在解决问题时,一般情况下都要用到,但有时有多
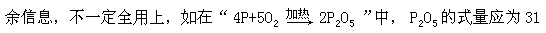
×2+16×5=142,而不应为 2×(31×2+16×5)=284。
-
化学试题中一般没有隐含条件,但有时也包含着隐含条件,如“KClO3
受热不再产生气体时,固体剩余物是纯净物还是混合物?”此题中就隐含着作为催化剂的 MnO2 这个条件,因此只能说得到的固体剩余物是混合物,而不能说是纯净物。
-
化学计算题中已知条件一般会有具体数据,但有时全题都是语言文字叙述,看来没有给出具体数据,这种无数据计算题并非真正的没有数据,而是把数据隐含在题目中,需要我们去寻找。例如:若
SO2 和 SO3 所含氧元素质量相等时,SO2 和 SO3 的质量比是多少?
分析:氧元素质量相等是联系 SO2 和 SO3 的“桥梁”,从而得出 SO2 和 SO3 之间的关系式。
解 :3SO2—60—2SO3 192 160
则 192∶160=6∶5
答:若 SO2 和 SO3 所含氧元素质量相等时 SO2 和 SO3 的质量比为 6∶5。
