教 学 过 程 :
|
教学程序 |
教学内容 |
教 师 活 动 |
学 生 活 动 |
|---|---|---|---|
|
一 、迁移阅读 |
实验室里制取气体的设计思 路 |
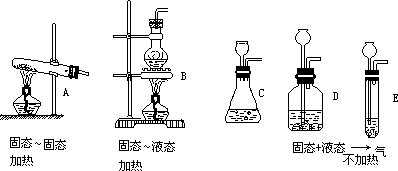
【复习】我们已学过O2、H2 的实验室制法(出示装置图),请同学们选择实验室制O2 、H2 的反应、收集装置图。 【设问】1.(出示幻灯)这装置能否制取CO2 (不要求回答) 2.在实验室里制取气体要考虑哪些问题?指导学生阅读课本P92 后回答问题 【板书】实验室里制取气体的设计思路: 1. 反应原理(原料条件等), 2.装置, 3.验证气体。 |
(1)口答选择装置图序号(2)悬念激思 (3)阅读教材用笔划要点(4)口答气体的设计的思路 |
|
二 、直观明理 |
一 、实验室制取二氧化碳的反应原理 |
【引言】今天我们按以上三点设计思路一起探讨CO2 的制取。首先探讨实验室制取CO2 的反应原 理,请同学阅读教材,了解反应物及反应需要条件和反应方程式。 【板书】一、实验室制取CO2 的反应原理 【设问】实验室是否可以用Na2CO3 代替石灰石; 是否可以用稀H2SO4 代替稀盐酸? 【展示】Na2CO3 、稀HCl 、大理石、稀H2SO4 【幻灯展示】 (1)Na CO + HC 2 3 l (2)CaCO3 + HCl 引导学生观 (3)CaCO3 + H 2 SO 4 察现象并比较产生气体的快慢。 【讲解】实验(1 )产生CO2 气体太剧烈,反应物很快用完,不适合实验室制取,适合灭火。实验(3 )开始有少量气体是因为生成了微溶物质, 防止了石灰石与硫酸进一步反应。因此实验室制取CO2 的反应物合适的是大理石与稀盐酸,指导 书 写 化 学 反 应 方 程 式 : CaCO3+2HCl=CaCl2+CO2 ↑+H2O |
(1 )学生围绕思路阅读了解制CO2 应原料、条件、反应方程式 (2 )激疑思考 (3 )了解物质状态(3 )观察现象并完成实验填空(见幻灯3 ) (5 )参与议论明确反应物选择缘故 (6 )静心听讲知道该化学方程的书写方法 |
|
四、 |
练 习 |
出示幻灯 5 、 6 思考讨论:
布置作业(作适当提示) 1.家庭实验(见课本 P94 ) 2.P96 习题 1 、 3 、 5 |
|
|---|---|---|---|
|
巩 |
( 1 )口答教师提出 |
||
|
固 |
的问题 |
||
|
深 |
( 2 )完成练习 |
||
|
化 |
板书设计:
第四节:二氧化碳的实验室制法
实验室里制取气体的设计思路: 1.反应原理(反应物状态、条件)
-
装置(收集)
-
验证气体
一、实验室制取二氧化碳的反应原理:
-
反应物名称:石灰石(或大理石)、稀盐酸。
-
常温下反应。
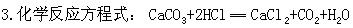
二、实验室制取二氧化碳的装置:
-
装置(同制氢气相似)所需仪器:锥形瓶、长颈漏斗、导气管、集气瓶。
-
选择二氧化碳反应装置规律:固态+液态—气
-
收集方法:向上排空气法(CO2 密度>空气,能溶于水与水反应)
-
验满方法:将燃着木条移近瓶口,木条熄灭证明 CO2 集满。
-
鉴定方法:将生成气体通入澄清石灰水,若变混浊证明该该气体为CO2。
三、实验室里制取二氧化碳步骤:
1.连接装置、检气密性 2.大理石放锥形瓶
3.向长颈漏斗里注入稀盐酸 4.收集(检满)5.检验
投影幻灯设计
 投影
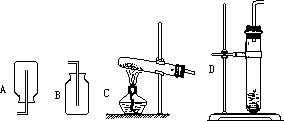
1:选择实验室制 O2、H2 反应装置及收集装置
投影
1:选择实验室制 O2、H2 反应装置及收集装置
投影 2:下列仪器装置能否制取 CO2?投影 3:完成下列实验填空
| 实验 | 主要现象 | 结论 |
|---|---|---|
| 碳酸钠与稀盐酸 | ||
| 石灰石与稀盐酸 | ||
| 石灰石与稀硫酸 |
投影 4:讨论题
-
怎样确定制取气体的装置,为什么可以用这装置制取 CO2?
-
装置中的长颈漏斗能否用普通漏斗代替,可用其它仪器代替锥形瓶吗?
-
怎样收集 CO2,为什么?又怎样证明 CO2 已充满集气瓶?
-
如何检验生成的气体是 CO2?
投影 5:思考题:若用固体硫化亚铁跟稀盐酸在常温下反应,制取硫化氢气体(H2S 能溶于水),应选用与 气体相同的反应装置,与 气体的收集装置相同。
投影 6:下列反应装置各有特点,实验室制 CO2 的反应装置可以是 。