-
腐植质形成的螯合物
- 腐植质的生成及其主要成分
约在 1800 年前后,人们方始在土壤和水体中发现有腐植质存在。由于组成和结构非常复杂,所以对它的化学性质等方面迄今还不十分了解。但长期以来,人们对它的研究兴趣却一直有增无减,目前,腐植质化学已经成为化学上的一个分支学科。
腐植质的环境化学意义在于:①存在于天然水体(或土壤)中的腐植质对金属离子有螯合作用,对有机物有吸附作用,成为水(或土壤)的天然净
化剂;②在加工生产饮用水的氯化过程,原水中腐植质与药剂 Cl2(及其中所含 Br2)反应,可生成三卤甲烷类化合物(THMs),具有强致癌性,成为公众健康的一大隐患;③水体中的腐植质可能作为光敏物质参与光化学氧化还原反应。
一般地说,腐植质首先在土壤中生成。土壤中生物体,特别是植物死亡后,在各种环境条件下分解后残留物就是腐植质。腐植质在土壤中广泛存在, 由于土壤和水体相通,不难理解,在水体和沉积物中也必然存在着相当数量的腐植质。但也有研究者指出,海水中所含腐植质,有部分是在该水体系统中直接生成的。土壤中腐植质形成的过程如下所示。作为起始物的植物和动物残体大致通过化学分解和微生物分解最终转为腐植质。
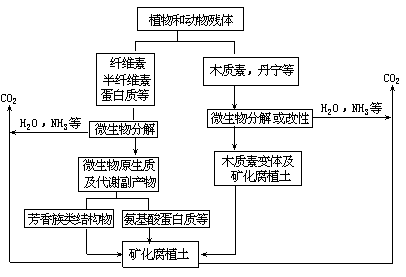
海水中腐植质含量约占有机物总量的 6%~30%,一般在 100~300μg/L范围之内。海水中腐植质经用高分子多孔聚合物 XAD-2 吸附浓集后,所得提取物再用酸碱按下列程序处理,即可获得腐植质的三种重要组分:
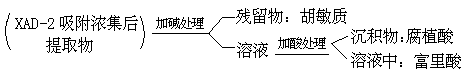
其中:①腐植酸,是能溶于碱而沉积于酸的组分;②富里酸,是兼能溶于酸和碱的组分;③胡敏质,是酸、碱皆不溶的组分。
- 腐植质的化学结构
腐植质具有非常复杂的化学结构,而且结构还随其来源(如土壤、淡水、海水、褐煤、沉积物)而异。其中最简单的富里酸的结构如图 4-17(a)所示。同图(b)中给出腐植酸结构模型。据信,腐植酸分子核心是一个含大量有机杂原子基团的高分子化合物,核心外围联结很多功能基因。
腐植质三种组分间的区别在于分子量和官能团含量的不同。如腐植酸和胡敏质比富里酸有更高的分子量和较少的亲水官能团。总的来说,腐植质的结构中含有羧基、酚基、醇基、羰基等官能团,其结构特点是:
-
以碳链为骨架,以—O—,—N—为交联基团;
-
含氢键,带有很多含氧功能基;
-
分子量大,如胡敏质、腐植酸分子量可达几万;
-
分子内多处带有电荷,高度极性;
-
分子内含蛋白质类和碳水化合物类的部分很容易发生水解;芳香核部分不易发生化学降解和生物降解。
- 由腐植质形成螯合物
腐植质对环境中几乎所有金属离子都有螯合作用,对于过渡金属尤为如此。对金属螯合能力强弱一般符合欧文-威廉(Irving-William)次序即:
Mg<Ca<Cd<Mn<Co<Zn≈Ni<Cu<Hg
表 4-11 列举了各种来源的腐植质与金属阳离子形成螯合物的稳定常数。
由表列 K 值大小可见,多数金属与腐植质形成螯合物不够稳定。在某些环境条件下,螯合物发生离解而使金属转为自由离子,即转为易被水生生物摄取的化学形态。
表 4 — 11 腐植质与金属离子螯合物的稳定常数
|
腐植质试样来源 |
logK |
||||||||
|---|---|---|---|---|---|---|---|---|---|
|
Ca |
Mg |
Mn |
Co |
Ni |
Cu |
Zn |
Cd |
Hg |
|
|
湖水 |
3.95 |
4.00 |
4.85 |
4.83 |
5.14 |
9.83 |
5.14 |
4.57 |
19.4 |
|
河川水 |
— |
— |
— |
— |
— |
9.59 |
5.41 |
— |
21.1 |
|
海水 |
3.60 |
3.50 |
4.45 |
4.83 |
5.41 |
8.89 |
5.27 |
— |
18.1 |
从海洋沉积物中分离出的腐植质,其对金属的总螯合容量约 97 ~ 150mg/g;对于不同金属,Cu、Zn、Ni、Co、Mn,螯合容量分别为 67.4、26.1、
17.4、9.6、5.6mg/g。
腐植质与金属生成的螯合物一般都不溶于水。富里酸与金属生成的螯合物相对易溶些,当[FA]/[Me]>2 时,倾向于易溶。
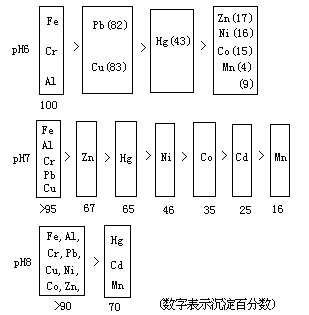 在
pH=6~8
范围内。天然水中各金属离子与富里酸生成螯合物的可溶程度如下所示。一般地说
Fe3+、Cr3+、Al3+、Pb2+、Cu2+的螯合物更为难溶,所以这些螯合物容易在土壤或沉积物中富集累积。
在
pH=6~8
范围内。天然水中各金属离子与富里酸生成螯合物的可溶程度如下所示。一般地说
Fe3+、Cr3+、Al3+、Pb2+、Cu2+的螯合物更为难溶,所以这些螯合物容易在土壤或沉积物中富集累积。
腐植质与金属间的螯合方式有以下几种:
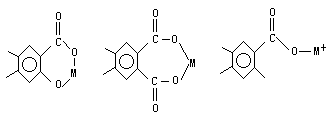
左边一种形式是以一个羧基和一个酚羟基螯合金属离子,中间一种形式是以两个羧基螯合金属离子,右边一种形式是以一个羧基与其配位络合。
