多核羟基络合物
金属离子在溶液中生成氢氧化物或羟基络离子的过程,实际上是水解过程,例如
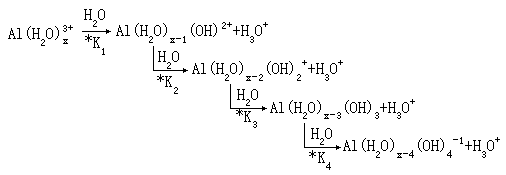
以上每步离解过程都是水中铝离子的酸性离解。P*K 的实验值为 12.4,
若将前面的各级离解常数*K 、*K 、*K 用*K 表示,其数值可以很粗略地按下式计算:
p*K =p*K -3(4-m),m=3,2,1
由以上水解过程可知,水合离子本身可以看作是一种以 H2O 分子作为配位体的络离子,因此,上述过程也就是络离子中的配位体逐步由 H2O 转化为OH-的置换过程。这一水解过程或者络离子转化过程,又是一种不断放出质子H+使溶液酸性加强的反应,所以它的进行程度和平衡状态与溶液的 pH 值直接有关。
铝和铁等金属离子的水解不只是到生成单核络合物为止,它们水解的最
终沉淀产物实际上是具有多核形态的结构,即借羟基作为中介,把各单核络合物的金属离子结合起来成为多核络合物,例如:
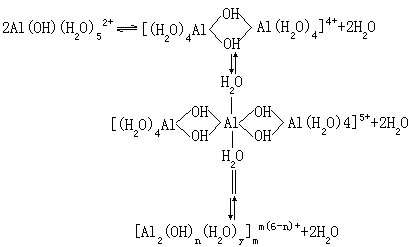
通过羟基桥联而生成多核络合物的过程中放出水分子,使生成物的配位水减少,这是由于羟基桥联后同时占用了两个金属离子的配位数。同时,生成物的电荷却增大了,由于静电相斥作用,这将会阻碍络离子的进一步结合。不过,多核络离子仍然会按水解方式继续反应,这种反应将使生成物的电荷降低,例如
 [Al3(OH)4(H2O)10]5+
[Al3(OH)5(H2O)9]4++H+
[Al3(OH)4(H2O)10]5+
[Al3(OH)5(H2O)9]4++H+
 [Al
(OH) (H O) ]6+ [Al (OH) (H O)
]4++2H+
[Al
(OH) (H O) ]6+ [Al (OH) (H O)
]4++2H+
络离子的电荷降低,并且羟基数目增多,都有利于进一步羟基桥联,生成更高级的多核络合物。这里的水解和羟基桥联两种反应交替进行,其最终结果则是生成难溶的氢氧化铝沉淀。
[Aln(OH)3n]—→[Al(OH)3]n↓
除 Fe3+和 Al3+外,许多金属离子如 Zn2+、Cu2+、Mg2+、Pb2+、Hg2+、Sn2+ 等,也都具有生成多核络合物的特性。人们利用这种特性将一些金属盐类用作混凝剂进行废水处理,取得了很好效果。常用的无机金属盐类混凝剂列举于表 4-10 之中。
表 4 — 10 各种无机混凝剂
|
类别 |
名称 |
分子式 |
略记号 |
使用 PH 值 |
|
|---|---|---|---|---|---|
|
硫酸铝 |
Al (SO ) · 18H O 2 4 3 2 |
AS |
6.0 ~ 8.5 |
||
|
低分子 |
氯化铝 |
AlCl 3 |
AC |
6.0 ~ 8.5 |
|
|
铝盐 |
含铁硫酸铝 硫酸铝钾 |
Al (SO ) +Fe (SO ) 2 4 3 2 4 3 Al (SO ) · K SO · 24H O 2 4 3 2 4 2 |
MIC KA |
6.0 ~ 8.5 6.0 ~ 8.5 |
|
|
聚硫酸铝 |
[ Al2 ( OH) n ( SO 4 ) n ] m 3− 2 [Al (OH) Cl ] 2 n 6-n m |
PAS |
6.0 ~ 8.5 |
||
|
高分子 |
|||||
|
聚氯化铝 |
PAC |
6.0 ~ 8.5 |
|||
|
硫酸亚铁 |
FeSO · 7H O 4 2 |
FSS |
8.0 ~ 11 |
||
|
低分子 |
硫酸铁 |
Fe (SO ) · 2H O 2 4 3 2 |
FS |
4.0 ~ 11 |
|
|
铁盐 |
三氯化铁 |
FeCl · 6H O 3 2 |
FC |
4.0 ~ 11 |
|
[ Fe ( OH) ( SO ) ] 2 n 4 n m 3 − 2 [Fe (OH) Cl ] 2 n 6-n m |
|||||
|
聚合硫酸铁 |
PFS |
4.0 ~ 11 |
|||
|
高分子 |
|||||
|
聚氯化铁 |
PFC |
4.0 ~ 11 |
|||
|
消石灰 |
Ca(OH) 2 |
CHO |
|||
|
其他 |
低分子 |
氧化镁 |
MgO |
MO |
9.5 ~ 14 |
|
碳酸镁 |
MgCO 3 |
MC |
9.5 ~ 14 |
