-
活性氧自由基
- 自由基及其性质
自由基被定义为在电子外层有未成对电子的分子、原子或基团。如氧分子具有两个未成对电子,可被看成双自由基。又例如氧分子或水分子在光照下可发生共价键均裂,从而产生成对的自由基:
O hv→ O· + O·
H O hv→ H· + HO·
处于自由基外层中的未成对电子对于外来电子有很强亲和力,故能起强氧化剂作用。在自然环境中,进入大气的微量气体多是还原态的,如 H2S、NH3、CH4 等,在滞留大气期间,它们受自由基氧化,待到返回地表时,就转化为高氧化态物质,如 H2SO4、HNO3、H2CO3 等。自由基的另一特点是它们有进行链式反应的倾向。因为自由基有未成对电子,它们与电子成对的分子发生反应后必然产生另一种自由基。因此自由基与分子间反应都是自行维持, 不断进行的,即由此引起链式反应。一般地说,自由基链式反应历程包括:
①引发,在此过程中自由基由某种起因(在大气中通常是阳光辐射)而产生;
②传播,发生自由基-分子反应,并延续一段过程;③终止,通常因自由基间复合、消失从而终止反应。以甲烷的光氯化反应为例,三阶段中发生的反应为:
引发 Cl2
hv→ 2Cl·
传播 Cl·+CH4→HCl+CH3· CH3·+Cl2→CH3Cl+Cl· CH3·+CH3Cl→C2H6+Cl·
终止 CH3·+Cl·→CH3Cl Cl·+Cl·→Cl2 CH3·+CH3→C2H6
对于对流层大气化学有重要意义的一类自由基是活性氧自由基,包括氢氧自由基 HO·、烷氧自由基 RO·、过氧自由基 HO2·、RO2·和过氧阴离子自由基 O2-·等,它们都是大气光化学反应产物。一般,在未污染对流层,活性氧自由基中以 HO·自由基浓度相对较高,且与其他组分发生氧化反应的能力较强。
在对流层空气中 HO·浓度约为 8.2×10-14(V/V),在低纬度地区浓度较高。
HO·的基本性质如下:
电子构型 1σ2,2σ2,3σ2,1π3,不成对电子进入 2p 轨道平均核间距 0.09706nm
键能 4.621eV(446kJ/mol) 偶极矩 1.66D
v 3 735cm-1
氧化还原电位 2.85V(HO·+H++e-H O)
活性氧自由基在调节大气中微量组分浓度的过程中起着很大的作用。但因为这些自由基的浓度非常低,与各种大气组分发生各种反应的机理又非常复杂,所以我们的认识一般还只局限在它们之间所发生的均相反应。在实验室进行有关的研究工作也存在着许多难点,例如反应器壁效应的影响、反应产物和中间生成物的定性、定量测定等方面都是实验室工作难点所在。
- HO·自由基在大气中的生成和清除反应在高层大气中 HO·生成反应为:
H O hv→HO· + H·
在未污染对流层中 HO·生成的主要途径是
O hv→O(1D)+O
O(1D)+H O→2HO·
在实验室中通常以如下两种反应途径获取 HO·自由基:
HONO hv→ HO· + NO 或 H2→2H·(低压条件下) H·+NO2→HO·+NO
HO·在对流层中自然发生的各种生成反应和消除反应归纳如下:
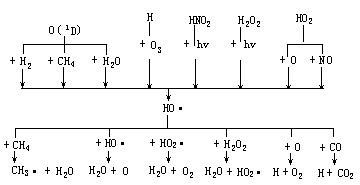
- HO·自由基与大气中有机物反应
大多数活性氧自由基对脂肪族结构化合物显示出相似的化学行为。但对芳香族和杂环化合物来说,不同的自由基所显示的化学行为也不一样。以HO·为例,活性氧自由基氧化有机物的基本过程约有三类:
(1)H 原子转移
- 在双键上加成
HO·+CH4→CH3·+H2O
HO·+C2H4→HOCH2CH2·
- 在芳香环上加成:
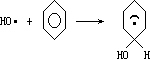
在反应式(1)中生成碳自由基能进一步发生下列反应
CH · + O 快 CH O ·
3 2 → 3 2
CH3O2·+HO2·→CH3OOH+O2
HO·自由基对大气中有机物的氧化反应速率可用下式表示: Rox≈kHO[C][HO·] (7-6)
式中 kHO——氧化反应速率常数; [C]——大气中被氧化有机物的浓度。
由于 HO·在对流层中有相对浓度较高和氧化能力最强等特点,所以在此未考虑其他氧化自由基的作用。由 HO·引发的各种有机化合物氧化反应的 kHO 列
于表 7-4 中。
表 7-4 大气中 HO ·氧化有机物的速率常数( 25 ℃)
|
化合物 |
10-9k ①( mol-1s-1 ) HO |
T ( d ) 1/2 |
|---|---|---|
|
正烷烃( C3 ~ C8 ) |
1.3 ~ 5.0 |
1.3 ~ 4.3 |
|
异烷烃( C6 ~ C10 ) |
0.6 ~ 2.9 |
1.9 ~ 9.4 |
|
环烷烃( C4 ~ C6 ) |
0.7 ~ 4.1 |
1.4 ~ 8 |
|
卤代甲烷( 1 ~ 3 氟或氯) |
1.2 (-4 )~ 0.065 |
87 ~ 47000 |
|
卤代乙烷( 1 ~ 3 氯或 3 ~ 4 氟) |
6 (-3 )~ 0.23 |
24 ~ 950 |
|
丁酮 |
1.9 |
2.9 |
|
醚( C2 ~ C6 ) |
2.5 ~ 1.0 |
0.6 ~ 2.2 |
|
烯烃(双键在端处)( C2 ~ C7 ) |
4.6 ~ 34 |
0.2 ~ 1.2 |
|
内烯烃( C2 ~ C5 ) |
29 ~ 98 |
0.06 ~ 0.2 |
|
苯 |
0.82 |
6.8 |
|
甲苯 |
3.5 |
1.6 |
|
二甲苯 |
5.9 ~ 12 |
0.47 ~ 1.0 |
① 速率常数栏中括号内数字为幂指数
当需要深入研究某有机物在大气中被氧化的反应速率问题时,应着重考虑下列三个方面:①大气中各种氧自由基或其他氧化剂的种类和浓度;②对象有机分子上某一特定基团被每一种氧化剂氧化的反应速率常数;③氧化过程中每一步的动力学机理。
- HO·自由基的检测方法
确定大气中 HO·自由基浓度的方法有三类,即计算法、化学法、物理法。现分述如下。
- 计算法和化学法
已知大气中下列组分浓度:H2O2、HCHO、H2O、O3、CO、CH4、NO 等,并已知温度和太阳辐射强度等参数的条件下,运用大气的光化学模型,可以通过电子计算机计算大气中 HO·的浓度。由于上述这些微量组分的准确浓度难以测得,所以人们对通过这样计算而得到结果的准确性也是怀疑的。但将由
这种方法所得到的结果作为实验测定方法的佐证,还是具有一定意义的。 化学测定法是在烟雾反应器中充入空气及 10-6(V/V)浓度级的烃类化合
物和 NOx,在紫外光照下,测定反应器中各种组分浓度随时间而变化的情况,
由此来推算 HO·的浓度及浓度的变化。这种方法在研究光化学烟雾生成机理方面有实用意义。
- 物理法
在这里我们简单介绍能直接测定大气中 HO·浓度的激光荧光法和长光程吸收法。
激光荧光法的测定装置如图 7-7 所示。这种方法以激光为光源,激发HO·自由基发射荧光,由荧光强度而求得 HO·自由基的浓度。如图 7-7 所示, 使用可调染料激光器,光束经过晶体倍频,获得波长为 282.5nm 的激光束。被 HO·自由基共振吸收后再发射出波长为 309nm 的荧光信号,该信号的强度
(s)与大气样品中 HO·浓度成正比:
s=AnσaηF (7-7) 式中 A——测量效率;
n——HO· 浓 度 ; σa——HO·对外来光子的吸收截面;
ηF——发射荧光的效率。
应用这种方法,首次实测了大气中 HO·的浓度,方法检测限为 5×106 个 HO·/cm3。
长光程吸收法是将波长为 307.9951nm,光束宽度小于 0.002nm 的激光束,由实验室射入空气,经过近 10km 射程并被 HO·自由基吸收衰减后,通过反射器返回实验室接收,由射出和返回的激光束强度变化,可以推算出大气中 HO·自由基的浓度。
