-
水体中的芳烃类和酚类污染物
-
水体中的芳烃类污染物
- 来源和基本性质
-
芳烃是芳香族化合物的母体,大多数芳烃含有苯的六碳环结构。对含苯环的芳烃根据所含苯环数目和联结方式不同,又可分为:①单环芳烃,其分子中只含一个苯环,如苯及苯的氯、硝基、甲基、乙基等取代衍生物;②多环芳烃(简写为 PAH),其分子中含有两个或两个以上苯环,如联苯、萘、蒽等。
存在于环境中的单环芳烃基本上只有人为来源,且主要来源于含多量单环芳烃的化石燃料。煤干馏、石油裂解或芳构化等加工过程中可产得多种单环芳烃,它们在生产、运输、销售、应用等过程中又会转入大气(单环芳烃多具有挥发性)或水体环境。所以水体中单环芳烃主要来源于工业废水、城市污水及倾翻入水体的原油。
存在于环境中的多环芳烃有天然和人为的两种来源。前者包括:①某些细菌、藻类和植物的生物合成产物;②森林、草原燃起的野火及火山喷发物;
③从化石燃料、木质素、底泥等散发出多环芳烃,是长期地质年代间由生物降解物再合成的产物。人为来源主要有:①废物焚烧和化石燃料不完全燃烧产生的烟气(包括汽车排气);②工厂(特别是炼焦、炼油、煤气厂)排出物。特别值得提及的是从吸烟者喷出的烟气中迄今已检测到 150 种以上多环芳烃,且其含量比饮水高得多。因此水体中多环芳烃主要来源于各类工业废水、大气降落物、表面敷沥青道路的径流及污染土壤的沥滤液等。与地下水、湖水相比,河水更易受污染,其中多环芳烃的浓度水平可能高于 0.05μg/L, 且多量被吸附在悬浮粒子上,仅少量呈溶解态。
芳烃类化合物的物理性质及化学稳定性主要由其分子结构中共轭π电子体系决定。水体中常见芳烃类化合物的一些特性参数列举在表 6-6 之中。
一些单环芳烃化合物仅微溶于水,在天然水体中滞留时间很短。随着苯环上取代氯原子数增多,化合物在水中溶解度降低,而在正辛醇/水体系中分配系数 Poct 增大。一般在苯环上引入氯原子还可引起熔点降低,沸点升高, 所以邻位和间位的二氯取代物呈液态的温度范围变宽。但对位的取代物呈相反的趋向。被氯取代后的苯环有较大化学反应性,但所有氯苯化合物都是热稳定性的。
表 6 - 6 芳烃类化合物的物理常数
|
化合物 |
分子式 |
分子量 |
熔 点 (℃) |
沸点(℃) |
相对密度 (d 20) 4 |
蒸气压* (Torr**) |
水溶 |
|---|---|---|---|---|---|---|---|
|
苯 |
C H 6 6 |
78 |
5.5 |
80.1 |
0.88 |
74.3 |
1780 |
|
氯苯 |
C H Cl 6 5 |
113 |
-45.6 |
131.7 |
1.11 |
8.8 |
472 |
|
1 , 2-二氯苯 |
C6H4Cl2 |
147 |
-17.0 |
180.5 |
1.31 |
1 |
100 |
|
1 , 3-二氯苯 |
C H Cl 6 4 2 |
147 |
-24.8 |
173.0 |
1.29 |
3 |
123 |
|
1 , 4-二氯苯 |
C H Cl 6 4 2 |
147 |
53.1 |
174.1 |
1.25 |
0.5 |
87.2 |
|
甲苯 |
C H 7 8 |
92 |
-95 |
110.6 |
0.87 |
22.4 |
515 |
|
邻二甲苯 |
C H 8 10 |
106 |
-25.1 |
144.4 |
0.88 |
5.2 |
175 |
|
乙基苯 |
C H 8 10 |
106 |
-95 |
136.2 |
0.86 |
7.1 |
152 |
|
硝基苯 |
C H NO 6 5 2 |
123 |
5.7 |
210.9 |
1.20 |
0.27 |
205. |
|
萘 |
C H 10 8 |
128 |
80.2 |
211 |
1.14 |
0.05 |
31.7 |
|
蒽 |
C H 14 10 |
178 |
216.2 |
340 |
1.25 |
1.7 × 10-5 |
0.04 |
|
( 25 ℃) |
( 25 |
||||||
|
菲 |
C H 14 10 |
178 |
100 |
340 |
1.025 |
9.6 × 10-4 |
1.00 |
|
( 25 ℃) |
( 25 |
||||||
|
■ |
C H 18 12 |
228 |
254 |
488 |
1.274 |
6.3 × 10-9 |
1.8 |
|
( 25 ℃) |
( 25 |
||||||
|
苯并[a]芘 |
C H 20 12 |
252 |
179 |
310-312 |
- |
5.6 × 10-9 |
3.8 |
|
(1.3kPa) |
( 25 ℃) |
( 25 |
* 20 ℃ ** 1Torr=133.3Pa
多环芳烃类化合物具有大的分子量和低的极性,所以大多是水溶性很小的物质,但若水中存在有阴离子型洗涤剂(如月桂酸钾)时,其溶解度可提高到 104 倍。含 2 至 3 个环且较低分子量的 PAH(萘、芴、菲、蒽)有较大挥发性以及对水生生物有较大毒性;含 4 至 7 个环的高分子量 PAH 化合物(■- 晕苯)虽然不显示出急性毒害,但大多具致癌性。
芳烃化合物在化学性质上表现惰性。一旦发生反应趋向于保留共轭环体系,即较容易发生与-Cl、-NO2、-SO3H、-CH3 等基团间的亲电子取代反应, 而难以发生加成或氧化反应。此外,PAH 可与水中存在的胶体形成复合物, 并以此形式在整个天然水系中迁移。因此曾在远离密集人群活动的海洋生物体组织中检测到了 PAH。
- 环境化学性质1)吸附
单环芳烃特别是氯代苯有较大 Poct 值(正辛醇-水分配系数),这表明它们能被沉积物中的有机组分强烈吸附。例如实验室研究表明,六氯苯在沉积物相和水相中的平衡浓度分别为 332μg/kg 和 8.3μg/L,浓集因子约 40。由于单环芳烃及其衍生物具有易被吸附的性能,致使其在水层中的浓度维持在较低的水平,并可使单环芳烃在水体中所发生的其他迁移或转化过程(如挥发)也有所减慢。
多环芳烃水溶性和蒸气压都很小,也容易被水中悬浮粒子或沉积物所吸
附。在水生生物中的浓度虽然比水中浓度要高几个数量级,但与沉积物中浓度相比还是较低的。低分子量 PAH 化合物通过沉积、挥发、微生物降解等过程而从水相中迁走;高分子量 PAH 化合物主要通过沉积和光化学氧化过程发生迁移和转化。人们受芳烃化合物具有易被吸附性能的启发,在废水处理中采用了混凝、沉降、过滤或活性炭吸附等方法,经试验也的确证实了这些方法的有效性。
- 挥发
对大多数单环芳烃化合物来说,决定其环境归宿的另一途径是朝大气方向的挥发。在挥发过程仅由气相动力因素控制的前提下,苯的挥发速率仅取决于水的温度。表 6-7 列举了一些典型单环芳烃化合物因挥发而迁移的半减期数据。但实际水体中对象物的半减期数据还与天然水体中水的深度及水的流速等因素有关。
表 6-7 典型单环芳烃因挥发而迁移的半减期
|
化合物 |
半减期(h) |
化合物 |
半减期(h) |
|---|---|---|---|
|
苯 |
4.81 |
乙苯 |
5~6 |
|
氯苯 |
9.0 |
硝基苯 |
~200 |
|
1,2-二氯苯 |
〈9.0 |
甲苯 |
5.18 |
|
1,3-二氯苯 |
~10 |
2,4-二硝基甲苯 |
~数百天 |
|
1,4-二氯苯 |
〈9.0 |
2,6-二硝基甲苯 |
~数百天 |
对于具有两个环的 PAH 化合物来说,有较大挥发性。例如飘浮海面的原油中所含的萘很容易在一定水温、水流、风速条件下挥发逸散到大气中去, 但存在于水体中具有 4 或 4 个以上苯环的 PAH 化合物在任何环境条件下都是不易挥发的。
包括很多芳烃(苯、甲苯、二甲苯、乙苯等)在内的许多有机物都具有易挥发特性。由此组成了一个有机化合物大类,被称为挥发性有机化合物类
(VOCs)。按世界卫生组织定义,凡有机物(不包括金属有机化合物和有机酸类)其在标准状态(293K 和 101.3kPa)下的蒸气压大于 0.13kPa 者即属VOCs 类化合物。所以除芳烃外还包括诸如四氯化碳、三氯乙烯等挥发性非芳烃类化合物。VOCs 类化合物因其低极性和高疏水性而易穿透土壤,进入地下水。且因地下水所具有的特殊环境条件,有可能使其进一步积聚到很高浓度水平,成为一组高危险性的污染物类。目前对 VOCs 类化合物的研究已经成为环境化学学科的一个专题。
- 水解、化学分解和光化学分解
在天然水体条件下,大多数单环芳烃不容易发生水解、化学分解或光化学分解。已知 2,4-二硝基甲苯是一个例外,在高度曝气的水中,它分子上的甲基能被水中溶解氧所氧化。在为处理废水而作的实验室研究中,应用Fenton 试剂(H2O2+Fe2+催化剂)能有力地使单环芳烃类化合物化学降解。若再外加紫外光照,则更能提高降解速率和降解程度。一般认为只是波长小于280nm 的入射紫外光才有可能引起分子光分解。
存在于大气中的 PAH 化合物较容易发生化学氧化或光化学氧化,但在溶液中就较难发生。表层水中的苯并[a]芘受光化学降解的能力主要取决于水中溶解氧浓度、温度和太阳光在水面上的辐射强度。在水下层光化学降解能力
显著减弱,因为一则光强减弱,再则温度和溶解氧浓度下降。至于被吸附在沉积物中的 PAH 化合物,其光化学降解就完全可以不计了。
- 生物降解
一些土壤和水生微生物能利用某些单环芳烃化合物作为碳源,所以苯、氯苯、1,2-二氯苯、六氯苯等都可能在水中为生物所降解。存在于土壤、污泥、海水中的微生物能对 PAH 化合物起降解作用,降解反应按一般芳烃化合物的降解机理进行,即先引入两个羟基,使 PAH 化合物转为二酚类化合物后再开环。此后,对低分子量 PAH 化合物可彻底降解转化为 CO2 和 H2O;对高分子 PAH 化合物则能产生各种代谢物酚和酸。
在哺乳动物的肝、脊椎动物或非脊椎动物的其他器官中存在着一种“多功能氧化酶(MFO)”,PAH 化合物能在这种酶的作用下降解,但由此产生的中间产物是具有致癌和致畸性的芳烃氧化物,由进一步降解才可转化为低毒的产物。
- 毒性
芳烃类化合物是高度脂溶性的,容易在人体富脂肪器官和乳液中累积。许多单环芳烃包括含 1 至 5 个氯原子的氯代苯、甲苯、乙苯、硝基苯都无致癌性。致癌或可能致癌的化合物有苯、2,6-二硝基甲苯、2,4,6-三硝基甲苯、偶氮苯、十二烷基苯等。顋鼠口摄六氯苯的试验表明,该化合物能引起肝肿、甲状腺腺瘤等症。此外,六氯苯还有致突变和对胎儿产生毒性等生理行为。
多环芳烃及其衍生物中很多具有致癌和致突变性,且致癌性与致突变性间有很好的相关关系。表 6-8 列举了某些致癌和不致癌的多环芳烃。除致癌性外,多环芳烃还可能损伤造血系统和淋巴系统。
表 6-8 多环芳烃的致癌性
|
致癌或可能致癌的化合物 |
苯并[a]芘,苯并[e]芘,苯并[a]蒽,苯并[a]荧蒽苯并[b]荧蒽,苯并[j]荧蒽、苯并[k]荧蒽, 苯并[g,h,i]苝,苯并[a]芴,■、芴、苝、芘 |
不 致 癌 化合物 |
苊烯、蒽、荧蒽萘、菲 |
- 含芳烃废水治理方法
含芳烃化合物的废水,例如石油化工废水都具有组分复杂(往往同时含有非芳烃类有机化合物,有时组分可多达上百种)、总有机碳量值高、水质变动大等特点。采用何种处理方法为合适不能一概而论,常因对象而异。一般情况下都需要进行三级处理方能达到最终净水目的,即达到地面水水质标准予以排放,或转为循环冷却水予以回收再用。
一级处理所用方法有沉淀、隔油、浮选、中和、均质、混凝沉降和气提等。隔油、浮选、混凝的主要目的是除油(内含多量不溶于水的芳烃),气提能除挥发性芳烃。二级生物处理可去除废水中可溶性芳烃。好氧生化处理法对大多数芳烃基本有效,它们能被活性污泥吸附并进一步分解。当芳烃上有取代基存在时会加快生化降解速度,例如甲苯要比苯更容易生化降解。某石油裂解工业废水中含致癌多环芳烃 1200μg/L,经生化处理后,其去除率约在 30%以上。三级处理方法主要有活性炭吸附、臭氧或过氧化氢氧化、萃取、离子交换等。
- 分析和检测
水样中芳烃类化合物的分析和检测一般都具有很大复杂性和技术难度,
在此只能作示例性或归纳性的阐述。1)单环芳烃的分析检测(示例)
对含 12 种单环芳烃化合物的水样用盐酸酸化后用苯萃取,再经过色层柱净化浓集,最后用气相色谱法(电子俘获检测器)分别定量。必要时还需要用气相色谱-质谱联用法(GC-MS)对单环芳烃组分作鉴定。12 种化合物的名称、它们的分析程序和分析结果分别见表 6-9 和图 6-10、图 6-11。
表 6-9 水样中待测组分
|
编号 |
名称 |
分子式 |
分子量 |
标准液浓度(mg/L) |
|---|---|---|---|---|
| 1 |
硝基苯 |
C H NO 6 5 2 |
123.11 |
0.2 |
| 2 |
邻硝基甲苯 |
C H NO 7 7 2 |
137.14 |
0.1 |
| 3 |
间硝基甲苯 |
C H NO 7 7 2 |
137.14 |
0.25 |
| 4 |
对硝基甲苯 |
C H NO 7 7 2 |
137.14 |
0.2 |
| 5 |
间硝基苯甲醚 |
C H NO 7 7 3 |
153.14 |
0.05 |
| 6 |
邻硝基苯甲醚 |
C H NO 7 7 3 |
153.14 |
0.2 |
| 7 |
对硝基苯甲醚 |
C H NO 7 7 3 |
153.14 |
0.4 |
| 8 |
2,6-二硝基甲苯 |
C H N O 7 6 2 4 |
182.14 |
0.05 |
| 9 |
间二硝基苯 |
C H N O 6 4 2 4 |
168.11 |
0.5 |
|
10 |
2,4-二硝基甲苯 |
C H N O 7 6 2 4 |
182.14 |
0.2 |
|
11 |
邻二硝基苯 |
C H N O 6 4 2 4 |
168.11 |
0.1 |
|
12 |
3,4-二硝基甲苯 |
C H N O 7 6 2 4 |
182.14 |
0.15 |
2)多环芳烃的分析检测
水体或废水中多环芳烃浓度低、种类多、分析技术复杂。以下 6 种常见化合物相对比较容易检测和分析,被定作为水中多环芳烃指示物。
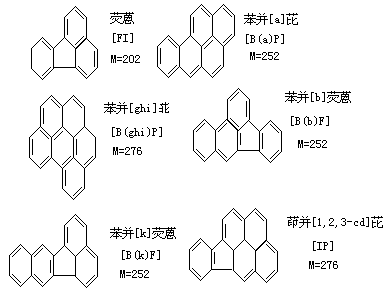
测定多环芳烃的主要方法有薄层层析法、气相色谱法和高效液相色谱法。近年来高效液相色谱法在国内外取得了最广泛的应用。对于水样先用环己烷萃取其中的 PAH,将萃取液以层析法通过硅胶柱作预分离。在以十八烷基硅烷(ODS)为固定相的液相色谱柱中,以甲醇/水为流动相,把经预处理
过的 PAH 分离成单个化合物,再用荧光分光(或紫外分光)检测器测定各化合物的峰高或峰面积,最后以外标法进行定量。应用此法测定 6 种多环芳烃指示物,它们的检测下限都可达到 ng/L 的数量级。
