《溶解度》课堂教学实施设计
【教学目标】
|
知识点 |
内容描述 |
水平 |
|---|---|---|
|
物质溶解性 |
易溶、微溶、不溶的区别和常见物质的溶解性 |
A |
|
溶解度 |
固体物质溶解度的概念,物质溶解度与外界条件的关系 |
B |
|
溶解度曲线 |
根据溶解度曲线,判断物质溶解度与温度的关系,查出物质的溶解度 |
B |
【教学方法】
启发讨论、自学评价
【教学结构】
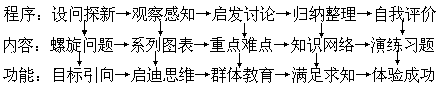
【教学程序】
[设问新探]
教师:前一节课我们学习了饱和溶液和不饱和溶液,请同学们思考什么叫饱和溶液?什么叫不饱和溶液?
学生:略
教师:请同学们再思考,饱和溶液在什么条件下,才具有确定的意义? 学生:是一定温度下,一定量的溶剂里。
教师:如果温度相同,溶剂的量也相同,不同的物质在溶液中达到饱和状态时所溶解的质量是否也相同呢?请同学们观察表 1。在 20℃,100 克水中达到饱和状态时,所溶解的质量分别是:NaCl36 克,KNO3 20.9 克、KClO37.4克、CaCO3 0.013 克,通过观察,可以得出怎样的结论?同座讨论。
学生:不同的物质在水中溶解的能力不相同。表 1(用幻灯片显示出来)
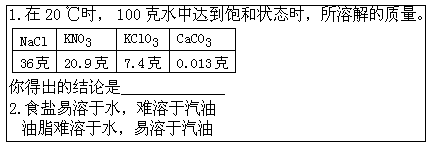
教师:我们把一种物质溶解在另一种物质里的能力,叫做溶解性。板书:物质的溶解性与哪些因素有关呢?(略)
学生:物质的溶解性与溶质、溶剂本身的性质有关。
[启发讨论]
- 引导学生观察教材上溶解度的概念,组织学生讨论:要正确理解这一概念,应抓住哪些要素?让学生回答提问,并板书,让学生默记概念一遍, 以得到巩固。
教师:为了准确的从量的方面表达物质的溶解性,就必须引入溶解度的概念(板书:溶解度。引导学生看教材 206 页黑体字),再组织学生讨论: 要正确理解溶解度的概念,应抓住哪些要素?
教师:(提问)正确理解溶解度的概念,应抓住哪些要素?(教师板书
(1)⋯(2)⋯(3)⋯(4)的内容)。
学生:(1)一定温度,(2)100 克溶剂,(3)饱和状态,(4)单位是克。
教师:以上四个要素中哪一个为可变要素? 学生:温度。
教师:请同学们默记溶解度概念。然后用图表展示下列问题,学生分组讨论,教师巡回指导。
表 2(用幻灯片显示出来)
教师:请同学们汇报一下讨论结果。
学生:(1)错误,没有说明饱和与否就不能说是溶解度。
-
错误, 100
克是溶液质量,不是溶剂克数,也没有说明饱和与否,说溶解度就不可以了。
-
错误,没有指明溶解度的单位是克数
-
错误:没有指明具体温度。
教师:在说明其物质的溶解度时,温度, 100 克溶剂,饱和状态、溶解克数四个要素是缺一不可的。请问: 20℃时食盐的溶解度是 36.5 克, 它表示的意义是什么?同座讨论。
学生:表示在 20℃时,每 100 克溶剂(水)中最多可溶解 36.5 克溶质
(食盐)或者表示在 20℃时,36.5 克溶质(食盐)溶解在 100 克溶剂(水) 中即可达到饱和状态。
教师:回答正确。
- 在学习溶解度概念以后,再继续学习其表示方法。
先设问,如果你测得 KNO3 在不同温度时的溶解度,你能否用一种既简略,又明了的方法记录下来呢?让学生回答出列表法之后,挂出一张表(KNO3 在不同温度下的溶解度),讲述这就是列表法。如果将这一张表沿中线裁开, 变换一下形式,就成了坐标法——溶解度曲线,讲解其制作方法,然后组织学生讨论:溶解度曲线可以表示出哪些意义,作适当讲解并板书。关于溶解性的划分问题是以学生自学、独立作业的形式进行的。
教师:我们学习了溶解度的概念,如何用数据把它表示出来呢?例如: 在 20℃时,KNO3 在 100 克水中达到饱和状态时,所溶解的质量是 31.6 克, 我们就说 20℃时,KNO3 的溶解度是 31.6 克。如果我们测定出了 KNO3 的不同温度下的溶解度,能否用一种既简略又明了的方法将数据记录下来较好。
学生:我认为列一个表格将数据记录下来较好。
教师:(展示一张图表)这种方法叫做列表法(引导学生进行观察表示
方式。板书:表示方法、列表法)表格内容如下:
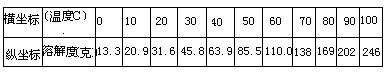
图 1 (用幻灯片显示出来)
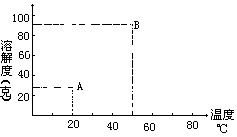
教师:如果我们将此表沿中线裁开用横坐标(b)表示温度,纵坐标(a) 表示溶解度,然后拼凑成直角,就成了坐标法,我们在图 1 上用一些点把不同温度时 KNO3 的溶解度描绘出来。比如,20℃时,KNO3 的溶解度是 31.6 克, 我们就描出了 A 点,反过来 A 点可以表示 KNO3 在 20℃时的溶解度是 31.6 克。
(提问)B 点可以表示什么意义?
学生: B 点表示在 50℃时, KNO3 的溶解度是 85.5 克。
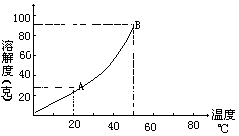 教师:如果我们将这些点连结成一条平滑的曲线,这样就作出了
KNO3 的溶解度曲线,如图 2,这就是 KNO3
的溶解度曲线。我们以同样的办法可以作出不同物质的溶解度曲线,
教师:如果我们将这些点连结成一条平滑的曲线,这样就作出了
KNO3 的溶解度曲线,如图 2,这就是 KNO3
的溶解度曲线。我们以同样的办法可以作出不同物质的溶解度曲线,
(稍停顿),下面请同学们仔细观察教材 208 页的图 7—1,7—2,讨论: 溶解度曲线可以表示哪些意义?(学生分组讨论,教师巡回指导)。
教师:请同学们汇报一下讨论结果。
学生:(1)同一物质在不同温度时有不同的溶解度。
-
不同的物质在同一温度时,溶解度不同(交点处表示的是两种物质在同一温度时溶解度相同)。
-
有些物质的溶解度受温度影响大,有些物质的溶解度受温度影响小。
-
大部分物质的溶解度随着温度的升高而增大,少数物质的溶解度随着温度升高而减少。
-
比较不同物质溶解度的大小。
教师:我们在制作溶解度曲线时,就知道同一物质在不同温度时,有不同的溶解度;不同的物质在同一温度时有不同的溶解度。交点表示不同物质在某一温度时的溶解度是相同的,比如大约在 70℃时, KNO3、NaNO3 的溶解度都是 138 克。我们从溶解度曲线的陡平来看,有些物质的溶解度受温度影
响很大,如 KNO3,从曲线上升或下降的趋势来看,大部分物质的溶解度随温度的升高而增大,也有极少数物质的溶解度随着温度的升高而减少,比如 Ca
(OH)2。我们根据溶解度曲线还可以比较不同物质的溶解度的大小,在 60
℃下列各物质的溶解度由大到小的顺序是怎样的呢?同座讨论。学生:硝酸钠>硝酸钾>氯化铵>氯化钾>氯化钠>硼酸。
教师:我们不仅可以比较大小,而且还可以根据溶解度的大小来区分物质溶解性,怎样来划分呢?请同学们先阅读教材 206 页的最后一自然段,然后分组讨论下列各题(用图表展示出来,教师巡回指导)。
表 4:(用幻灯片显示出来)
- 根据溶解度来划分物质的溶解性(20℃时)
| 溶解度(克) |
< 0.01 |
0.01 — 1 |
1 — 10 |
> 10 |
|---|---|---|---|---|
| 溶解性 20 (℃) |
- 70℃时 KCl 的溶解度是 克;
 (2)70℃时,NH4Cl
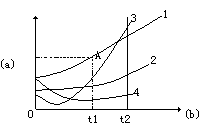
的溶解度是 克。3.观察下图填空。
(2)70℃时,NH4Cl
的溶解度是 克。3.观察下图填空。
(1)A 点的意义是 ;
-
在 t2 时,1,2, 3, 4 四种物质溶解度由大到小的顺序是 。
-
物质的溶解度受温度影响最大, 物质的溶解度受温度影响最小 ,
物质的溶解度随温度的升高而减小。
教师:请同学们汇报一下讨论结果。
[归纳整理]将本节学习的新知识整理成知识网络,然后对照教学目标引导学生自觉消化巩固,力求达到教学目标。
(略)
[自我评价]在课堂教学时间内,教师分发自我评价题,学生独立完成, 检测教学效果,教师了解教学现状,学生巩固开拓。
教师:请同学们用 5 分钟时间完成下列各题,并分发评价题。1.t℃时,某物质 M 的溶解度是 a 克,表明 t℃时 ,M 物质的质量是
。
-
查表,70℃,氯化钾的溶解度是 。它表示 克 中含 克和 克。
-
判断:
-
所有固体物质的溶解度都是随着温度升高而增大。
-
在 20℃时,100 克硫酸铜溶液里含有 10 克硫酸铜,硫酸铜的溶解度是 10
克。
-
20℃时, A 物质溶解在 10 克水中, B 物质 150 克溶解在 1000 克水里,A
比 B 的溶解度小。
学生:独立完成上述评价题。
教师:用集体评讲的方式,学生通过举手表示正误结果,教师统计正误率,以检查教学效果。
学生:反馈校正,同座讨论消化知识,形成技能技巧。
教师:本节课我们学习了固体物质的溶解度的有关知识,那么,气体物质的溶解度又怎样呢?请同学们课后思考。本课到此结束。下课。
(李德胜 毛全清)
