《单质、氧化物、酸碱盐相互关系》教案设计
本节教材是对无机物类别和相互关系的总结,也是初中化学的重点课型之一,学生学起来有一定难度,要上好这节课应体现两个意图:一是让学生对无机物分类和初中化学中常见的无机物有一个总体印象,系统了解;二是用图的形式总结和归纳各类无机物的相互关系,并运用关系图推测各类物质的主要化学性质和制取各类物质的可行方法。这节课是应用启发式教学的好教材,课堂上以学生活动为主,教师只起点拨、引导、调控作用。
这节课我是这样安排布局的:首先复习化学研究的对象是物质,引出了物质可分为纯净物、混合物两类,进而总结出下列无机物的分类表(该表教材上没有):
金属:Cu、Fe, k
单质非金属: P、S、C、O2 、H 2 ,
惰性气体: He, Ne
酸体气体物: CO2 、SO2
氧化物
碱性氧化物: CaO2 、Fe2O3
可溶性碱: NaOH 、Ba(OH )
纯净水
碱 2 2
难溶性碱: Cu(OH ) 2 、Fe(OH )2
化合物
含氧酸: H SO
、H S
酸
2 4 2
无氧酸: HCl、CuSO4
正盐: NaCl、CuSO
盐酸式盐: Ca(HCO3 )2 、KH2 PO4
碱式盐: Cu
(OH ) CO
2 2 3
以上表授课时可以引导学生自己总结。通过总结使学生对无机物分类的知识更加系统,并为以后学习元素化合物的知识打下基础。列出分类表后教师可用如下几句简短的语言导入新课:对无机物的分类我们已有了系统的了解,这些无机物之间有什么内在联系呢?让我们共同来学习本章的第九节,
单质、氧化物、酸、碱、盐的相互关系,通过列表导入新课向学生转达了当堂课的教学意图,勾画出所学知识的轮廓。学生迫切要求知道这些物质间究竟有什么相互关系,使学生的求知欲大增。变“要我学”为“我要学”。接着教师说明:为了研究问题方便我把上述分类表缩减成一幅简单的图形,根据图形来分析研究物质间的内在联系和在一定条件下的相互转化。我们简称该图为关系图:教师出示预先绘制好的图形,学生通过观察发现关系图确是分类表的简单表现形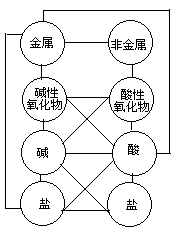 式,教师边讲边用不同的颜色画出四组(十二条)线,称为四横、两纵、两弯、四交叉,学生听起来既顺口又新鲜。又一次激发学生的学习兴趣,使学生的思维活跃起来,然后教师引导学生总结出这十二条线之间物质的关系,教师还可引导学生说出每一条线都代表一类化学反应。顺便让学生各举出一个有代表性的反应。
式,教师边讲边用不同的颜色画出四组(十二条)线,称为四横、两纵、两弯、四交叉,学生听起来既顺口又新鲜。又一次激发学生的学习兴趣,使学生的思维活跃起来,然后教师引导学生总结出这十二条线之间物质的关系,教师还可引导学生说出每一条线都代表一类化学反应。顺便让学生各举出一个有代表性的反应。
四条横线的内容:
金属+非金属—→无氧酸盐
Fe+S → FeS
碱性氧化物+酸性氧化物—→含氧酸盐
CaO = SiO2 ∆CaSiO2
碱+酸—→盐+水NaOH+HCl=NaCl+H 2 O 盐+盐—→新盐+新盐
NaCl+AgNO3=AgCI↓+NaNO3
两条纵线的内容:
+o2 + H2O +碱
金属 → 碱性氧化物 → 碱 → 盐
+O2 + H2O +碱
非金属 → 酸性氧化物 → 酸 → 盐
两条弯线的内容:
金属+酸—→盐+氢气 Zn+H 2SO 4 =ZnSO4 +H 2 ↑ 金属+盐—→新盐+新金属
Cu+Hg(NO 3)2 =Cu(NO 3)2 +Hg 四条交叉线的内容:
碱性氧化物+酸—→盐+水
Fe 2O 3 +6HCl =2FeCl3+3H 2 O
酸性氧化物+碱—→盐+水
CO 2 +2NaOH=Na 2 CO 3+H 2O
碱+盐—→新碱+新盐
2NaOH+CuSO4=Cu(OH) 2↓+Na 2SO 4
酸+盐—→新酸+新盐
HCl+AgNO3=HNO 3+AgCl↓
这些内容完成后,各类物质间的相互关系也就明确了,然后教师引导学生再仔细观察图形,从图上还可知道某一类物质的化学性质。如:酸的化学性质:
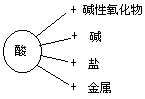
同样可知碱类、盐类的化学性质。另外,从图上还可归纳出各类物质的制取方法。其次还可根据两类的内容,复习金属活动性顺序的规律。根据图的最下边几种物质的反应,复习复分解反应发生的条件和规律。这样学生感到关系图虽简单,但包含的内容很多,他们就会自觉地去理解记忆该图,应用该图解决问题。从而培养学生的综合概念能力、分析问题解决问题的能力, 圆满地完成了教学任务。
通过这一节课的教学,学生可以利用关系图探究制取某种物质的可行方法。第二课时教师可引导学生从关系图中找出制取硫酸锌这种盐的五种适当的方法。再指导学生归纳总结出制取碱性氧化物、酸性氧化物、酸、碱的可行方法。每类物质都可举出一例让学生自己设计,反复练习。达到熟练运用,
牢固掌握反应规律的目的。
