第四节 主要污染物在水环境中的迁移转化
一、需氧污染物
需氧污染物主要指生活污水和某些工业废水中所含的碳水化合物、蛋白质、脂肪和木质素等有机化合物,在微生物作用下最终分解为简单的无机物质,即二氧化碳和水等。因这些有机物质在分解过程中需要消耗大量的氧气, 故又被称为需氧污染物。虽然需氧有机污染物没有毒性,但若水中含量过多, 势必造成水中溶解氧的减少,从而影响鱼类和其它水生生物的正常活动,需氧有机污染物是水体中普遍存在的污染物之一。
(一)需氧有机物的生物降解作用
需氧有机污染物一般分为三大类,即碳水化合物、蛋白质和脂肪,其它有机化合物大多为它们的降解产物。上述三大类物质的生物降解作用有其共同特点:首先在细胞体外发生水解,复杂的化合物分解成较简单的化合物, 然后再透入细胞内部进一步发生分解。分解产物有两方面的作用,一是被合成为细胞材料,二是变成能量释放,供细菌生长繁殖。
需氧有机污染物的生物降解过程比较复杂,根据各类化合物在有氧或无氧条件下进行反应的共性,可归纳出大致的降解步骤和最终产物。例如碳水化合物生物降解步骤和最终产物为:

碳水化合物是 C、H、O 组成的不含氮的有机物,可分为多糖[(C6H10O5)
n,如淀粉]、二糖[(C12H22O11),如乳糖]、单糖[(C6H12O6),如葡萄
糖]。在不同酶的参与下,淀粉首先在细胞外水解成为乳糖,然后在细胞内或细胞外再水解成为葡萄糖。葡萄糖经过糖解过程转变为丙酮酸。在有氧条件下,丙酮酸完全氧化为水和二氧化碳。在无氧条件下,丙酮酸不能完全氧化,最终产物是有机酸、醇、酮。对水环境影响较大的就是这部分产物。
脂肪和油类的生物降解步骤和最终产物为:
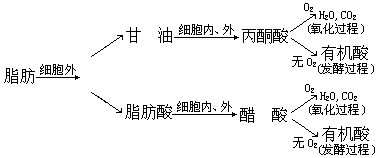
脂肪和油类的组成与碳水化合物相同,由 C、H、O 组成。脂肪的生物降解步骤和最终产物比碳水化合物更具多样性。脂肪首先在细胞外水解,生成甘油和相应的脂肪酸。然后上述物质再分别水解成为丙酮酸和醋酸。在有氧条件下,丙酮酸和醋酸完全氧化,生成水和二氧化碳,在无氧条件下,完成发酵过程,生成各种有机酸。
蛋白质的生物降解步骤和最终产物为:

蛋白质的组成与碳水化合物和脂肪油类不同,除含有 C、H、O 外,还含有 N。蛋白质是由各种氨基酸分子组成的复杂有机物,含有氨基和羧基,并由肽键连接起来。蛋白质的生物降解首先是在水解的作用下脱掉氨和羧基, 形成氨基酸。氨基酸进一步分解脱氨基,生成氨。通过硝化作用形成亚硝酸, 最后进一步氧化为硝酸。如果在缺氧水体中硝化作用不能进行,就会在反硝化细菌作用下发生反硝化作用。
一般来讲,含氮有机物的降解比不含氮的有机物难,而且降解产物污染性强,同时与不含氮的有机物的降解产物发生作用,从而影响整个降解过程。
(二)需氧有机污染物降解与溶解氧平衡
需氧有机污染物的降解过程制约着水体中溶解氧的变化过程,因此,研究此问题对进行水污染评价、水产资源危害及水体自净作用都有重要意义。50 年代,美国学者巴特希(A.F.Bartsh)和英格莱姆(W.M.Ingram)就编制出了关于被生活污水污染的河流中 BOD 和溶解氧(DO)相互关系的模式图(图6.7),在世界范围内被广泛应用。
该图简明醒目,非常清楚地反映出在被污染河流中 BOD 与 DO 之间沿程变化的曲线和根据 BOD 与 DO 变化曲线划分出该河段的水功能区(清洁水区、水质恶化区、恢复水区和清洁水区)。
在污染河流中耗氧作用和复氧作用影响着水中溶解氧的含量。耗氧作用指有机物分解和有机体呼吸时耗氧,使水中溶解氧降低;复氧作用(也称再曝气作用)指空气中的氧溶于水和水生植物的光合作用放出氧,使水中溶解氧增加。耗氧作用和复氧作用的综合决定着水中氧的实际含量。
图 6.7 某城镇生活污水流入河流后 DO 与 BOD 的变化
(流量 100m3/s,水温 25℃,人口 4 万)
(资料来源:陈静生等,环境污染与保护简明原理,1981) 需氧有机物分解与溶解氧平衡可用以下几种数学模式来描述:
- 耗氧作用定律早在 1944 年,斯特里勒(H.W.Streeler)和费尔普斯(E.B.Phelps)就曾指出:“有机物质的生物化学氧化率与剩下的尚未被氧化的有机物的浓度成正比”,此即为 Phelps 定律,经微分,积分,推得:
Lt = 10−kt 或L L t
= L10−kt
式中,L 为起始时的有机物浓度;Lt 为 t 时间后的有机物浓度;Lt/L 为剩余的有机物占起始时有机物的比率;K 为耗氧速度常数,以日计算,普通生活污水在 20℃时,K 值约为 0.1;t 为天数。
当 K=0.1,20℃时,水体中有机物的正常氧化速度见表 6.10。
从表 6.10 中可以看出,有机物的正常生化氧化速度是在第一天被氧化掉20.6%。似后每延续一天就从剩余的有机物中再氧化掉 20.6%。尽管氧化速率没有变,但每一天的氧化量却逐渐减少。
从表 6.10 中还可以看出时间的重要意义。在第三天末有机物氧化分解了50%,剩余的有机物也是 50%。因此可以认为,有机物生物分解的半衰期为三天。按此定律,又把剩余的有机物再分解 50%,即到第 6 天末,剩余的只
有 25%,依此类推,到 18 天末,有机物只剩下 1.6%。
表 6.10 有机物的在水体中的正常氧化速度(20℃,k=0.1 时)
|
日 数 |
占总有机物量的百分率 |
||
|---|---|---|---|
| 剩余量 |
当日氧化量 |
积累氧化量 |
|
|
0 |
100 |
20.6 |
0 |
|
1 |
79.4 |
16.4 |
20.6 |
|
2 |
63.0 |
13.0 |
37.0 |
|
3 |
50.0 |
10.2 |
50.0 |
|
4 |
39.8 |
8.2 |
60.2 |
|
5 |
31.6 |
6.6 |
68.4 |
|
6 |
25.0 |
5.0 |
75.0 |
|
7 |
20.0 |
4.2 |
80.0 |
|
8 |
15.8 |
3.3 |
84.2 |
|
9 |
12.5 |
2.5 |
87.5 |
|
10 |
10.0 |
2.1 |
90.0 |
|
11 |
7.9 |
1.6 |
92.1 |
|
12 |
6.3 |
1.3 |
93.7 |
|
13 |
5.0 |
1.0 |
95.0 |
|
14 |
4.0 |
0.8 |
96.0 |
|
15 |
3.2 |
0.7 |
96.8 |
|
16 |
2.5 |
0.5 |
97.5 |
|
17 |
2.0 |
0.4 |
98.0 |
|
18 |
1.6 |
0.3 |
98.4 |
|
19 |
1.3 |
0.1 |
98.7 |
|
20 |
1.0 |
99.0 |
(资料来源:陈静生等,环境污染与保护简明原理,1981。) 图 6.8 温度对 BOD5 分解过程的影响[kt=k20℃×1.047(t-20)]
(资料来源:同图 6.7。)
温度影响生物的活性,因此也就控制着有机物的分解速率。图 6.8 是不同温度对 BOD 分解过程的影响。
从图 6.8 中可以看出,曲线 A 是 20℃,k=0.1 时,半衰期为 3 天,BOD5 是 68%。当温度为 29℃时,k=0.15(曲线 B),半衰期为 2 天,BOD5 是 82
%。当温度为 14℃时,k=0.075(曲线 C),半衰期为 4 天,BOD5 是 58%, 这是耗氧过程的正常情况。但事实上耗氧过程是一个非常复杂的生化现象, 在自然界会受到其它因素的影响,出现偏离正常情况的现象。
- 复氧作用定律复氧作用受溶解定律和扩散定律的控制,即溶解速度与溶解氧低于饱和浓度的亏缺值成正比;扩散速度与河水中两点间的溶解氧浓度差成正比。根据这两条定律,Phelps 确定了静水中的复氧作用公式:
D = 100 − [(1− B )×81.06(e)−k
100
- e −9k
9
e−25k
25 )]
式中,D 为经复氧后的溶解氧含量(各深度的平均饱和百分数);B 为
π 2at
复氧开始时的溶解氧含量;K为常数,随
L 是水深(厘米),a 是扩散系数。
4L2
而定。t是复氧时间(小时),
Phelps 确定,at=1.42×1.1(t-20),20℃时,a 的平均值为 1.42。
- 河流溶解氧下垂曲线方程当有机耗氧污染物排入河流后,根据耗氧作用和复氧作用的综合效应,沿河流纵断面形成一条溶解氧下垂曲线(图6.9),它对评价河流污染及控制污染有十分重要的意义。
从图 6.9 中可以看出,在起始断面耗氧污染物排入河流后,耗氧速度最大,以后逐渐减少而趋向于零。复氧速度开始时为零,以后随氧亏值的增大而增大。水中溶解氧含量在某一时刻降至最低点,此点称为临界点。在临界点以后,复氧作用逐渐占优势,水中溶解氧含量开始上升。
图 6.9 溶解氧下垂曲线模式
1925 年,H.W.Streeler 和 E.B.Phelps 在研究美国 Ohio 河时,建立了BOD-DO 模型,常被称作 S-P 模型。该溶解氧下垂曲线计算公式为:
D = K1La
(10−k1 t− 10−k2 t ) + D
- 10−k 2 t
K 2 − K1
式中,D 为任一点的氧亏值;La 为初始 BOD 值;Da 为初始氧亏值;K1 为耗氧系数(常用对数表示);K2 为复氧系数(常用对数表示);t 为时间(日)。
K1 =
1 log La
∆t Lb
,K = K L −
2 1 D
∆D 2.3∆t D
式中,La 、Lb 分别为A、B点的BOD值;L为A、B两点间BOD的平均值;D为A、B两点间的平均氧亏值;△t为流经时间;△D为A点至B点的氧
亏变化。
临界时间 t
= 1 lg K 2 [1− Da (K 2 − K1 ) ]
K2 − K1 K1
临
La K1
临界氧亏
D = K1 L ×10−k1 tc
c a
2
自净速度
f = K 2
K1
表 6.11 列举了国内外某些河流的水质模型的 K1 和 K2 参数值,供参考。S-P 模型建立后得到了广泛应用。60 年代后,出现了各种修正的 BOD-DO
模型。模型的内容和形式也越来越复杂并都有其不同的使用要求。一般地讲,
模型越复杂越能较全面地反映河流实际情况。但这要增加许多建模参数,况且不同河流有不同的主要影响水质的因素。因此,片面强调选择参数多的复杂模型这种作法并不可取。对一条河段来说,选择模型的量和参数及模型复杂程度,应根据实际需要和目前所能获得的资料等几个方面进行综合考虑, 作出简便、经济、适当的选择。
