【实验 6—30】盐和另一种盐的反应
在一支盛有 3 毫升氯化钠溶液的试管里滴入几滴硝酸银溶液,在另一支
盛有 3 毫升硫酸钠溶液的试管里滴入几滴氯化钡溶液,观察有什么现象发生。
两支试管中都有白色沉淀产生。化学方程式如下:
NaCl+AgNO3→AgCl↓+NaNO3 Na2SO4+BaCl2→BaSO4↓+2NaCl
两种盐起反应,一般生成另外两种盐。
通过学习,我们知道了酸、碱、盐之间存在着相互反应的关系;从以上反应看,它们都是两种化合物相互交换成分,产生另外两种化合物的反应, 化学上把这类反应叫做复分解反应。如:
NaOH+HCl→NaCl+H2O CaCO3+2HCl→CaCl2+H2O+CO2↑
FeCl3+3NaOH→Fe(OH)3↓+3NaCl
如果把氯化钠稀溶液和硝酸钾稀溶液混合在一起,既没有沉淀析出,也没有气体放出或水生成,实际上并没有发生复分解反应。
中和反应是复分解反应的一种。
复分解反应发生的条件:即有的反应中生成沉淀,有的反应中生成气体, 还有的反应中生成水,只要具备这三个条件中的一条,复分解反应即能发生。
【习题】
一、用短线把下列各种盐的化学式跟它所属的类别连接起来。
|
正盐 酸式盐 无氧酸盐 |
NaCl NH4Cl NaHSO4 |
钠盐 铵盐 硫酸盐 |
|---|---|---|
|
含氧酸盐 |
NH4HCO3 |
盐酸盐 |
|
二、选择题。 |
-
今有失去标签的烧碱、食盐、盐酸三种溶液,只用一种试剂就能把它们鉴别出来,这种试剂是 ( )
-
锌粒
-
硝酸银
-
石蕊试液
-
胆矾
-
-
纯碱属于 ( )
-
碱
-
碱式盐
-
金属氧化物
-
正 盐 3.在盛有下列物质的烧杯里,加入过量的盐酸,能得到无色溶液的
是 ( )
-
氢氧化铜
-
苛性钠
-
硝酸银
-
氢氧化铁
4.下列反应属于复分解反应的是 ( )
(A)NH4HCO3
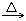 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
(B)CO2+C
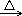 2CO
2CO
-
2HNO3+Cu(OH)2
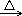 Cu(NO3)2+2H2O
Cu(NO3)2+2H2O -
Zn+CuSO4→Cu+ZnSO4 三、填空题。
- 有 A、B、C 三种金属,将 A 和 B 浸入稀硫酸中,A 溶解而 B 不溶解,
再将 C 浸入 A 的硝酸盐溶液中,其表面有 A 析出,则三种金属的活动顺序是
。
- 叫复分解反应,若能生成 ,或 ,或
,那么复分解反应就可以发生,否则就不能发生。
四、判断下列化学反应能否发生,能发生的写出化学方程式,不能发生的说明理由。
-
铜和碳酸钠溶液
-
盐酸和碳酸钡
-
氢氧化钾和硝酸铜溶液
-
氯化钡溶液和硝酸钠溶液
五、300 毫升稀盐酸(密度为 1.03 克/厘米 3、质量分数为 6%)和足量的硝酸银反应,生成氯化银的质量是多少?
