《食盐水电解》的两种教案设计
在教学内容、教学目的、实验手段、学生实际等教学常规问题都己明确、制订、了解以后,对于一个教师用不同的方法(注意,仅仅是方法不同); 对同类型的学生在相同的时间里去实现同一内容的教学会产生明显不同的效果。
以“讲授法”和“发现法”两种不同的教学方法在对食盐水电解的教学中展示这个客观事实。
在学生对电解质溶液通电,其中阴、阳离子分别在两电极放电顺序的知识了解以后,以三种不同的形式来进行对比教学。(各例举其主要过程)
方法 1,结合演示实验讲解

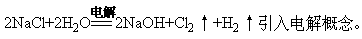 教师:食盐溶液中存在着水和食盐的电离
H2O H++OH-,NaCl=Na++Cl-通电以后阳离子 Na+、H+向阴极运动,根据放电顺序
H+在阴极被还原生成氢气,得出电极反应式:阴极
2H++2e→2H,2H→H2↑。Cl-、OH-向阳极运动,根据放电顺序 Cl-
在阳极被氧化生成氯气,得出电极反应式:阳极
2Cl-—2e→2Cl,2Cl→Cl2↑。清楚解释了由于 H+ 的放电使阴极区溶液中[OH-]>
[H+]而呈碱性,生成烧碱NaOH,得出电解方程式:
教师:食盐溶液中存在着水和食盐的电离
H2O H++OH-,NaCl=Na++Cl-通电以后阳离子 Na+、H+向阴极运动,根据放电顺序
H+在阴极被还原生成氢气,得出电极反应式:阴极
2H++2e→2H,2H→H2↑。Cl-、OH-向阳极运动,根据放电顺序 Cl-
在阳极被氧化生成氯气,得出电极反应式:阳极
2Cl-—2e→2Cl,2Cl→Cl2↑。清楚解释了由于 H+ 的放电使阴极区溶液中[OH-]>
[H+]而呈碱性,生成烧碱NaOH,得出电解方程式:
教师以严谨的教材组织,逻辑的语言,突出重点的讲解,透彻的分析、成功的演示,主要以自己讲授的方式进行教学。
学生:认真接受教师传授的知识。
对知识的迁移能力:①电解 KCl 溶液,学生尚能由食盐溶液为依据进行分析。②电解 H2SO4 溶液,学生不会。
在教师具体讲解例举几种不同类型电解质溶液的电解以后,学生会了。方法Ⅱ,结合演示实验,让学生思考
教师:提问,在食盐溶液中存在着哪几种离子?为什么?
学生:思考,得出结论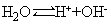 ,NaCl=Na++Cl-。(是对原有知识的再现。)
,NaCl=Na++Cl-。(是对原有知识的再现。)
教师:提问,当通电以后这些离子的运动状况怎样?
学生:复杂,得出结论阳离子 H+、Na+向阴极移动;阴离子 Cl-、OH-向阳极移动。
教师:提问,根据离子放电顺序,在阴极是哪种离子放电?
学生:思考,得出结论,H+与 Na+比较是 H+先放电被还原。师生一起写出电极反应式:阴极 2H++2e→2H,2H→H2↑。
教师:提问,根据离子放电顺序,在阳极是哪种离子放电?
学生:思考,得出结论,Cl-与 OH-比较是 Cl-先放电被氧化。师生一起写出电极反应式:阳极 2Cl—2e→2Cl,2Cl→Cl2↑。
教师:提问,为什么溶液的碱性,即[OH-]>[H+]是在阴极区呈现出来? 学生:静心思考以后,一部分学生能得出因为 H+在阴极放电以后,在
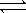 H2O
H++OH-的过程中,平衡向右移动而使阴极区[OH-]>[H+],溶液对指示剂呈碱性反应,生成
NaOH。
H2O
H++OH-的过程中,平衡向右移动而使阴极区[OH-]>[H+],溶液对指示剂呈碱性反应,生成
NaOH。
师生一起写出电解化学方程式:
2NaCl+2H2O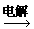 2NaOH+Cl2↑+H2↑得出电解的概念。
2NaOH+Cl2↑+H2↑得出电解的概念。
对知识的迁移能力:①电解 KCl 溶液,学生容易分析。②电解 H2SO4。溶液,以及其它不同类型的电解质溶液,学生能分析。
因为在Ⅱ法中,学生随着教师提出的问题通过自己思考得出的结论。Ⅰ
法中,学生的思维活动主要是意义识记的过程;Ⅱ法中学生的思维活动主要是分步再现、推理的过程。这是在二种不同的心理活动中完成的,前者是被动接受的心态,后者是发现探索的心态。
由于在Ⅱ法中教师所提的问题是用一般的原理、规律即对不同电解质溶液都可适用的问题去指导分析特殊的 NaCl 溶液的电解,学生在学习过程中就具有了一定的用一般规律去解决其它具体问题的能力,于是在知识迁移过程中表现出与Ⅰ法有明显的差别。
方法Ⅲ,高层次的演示法
在有条件的情况下,可做学生实验,在无条件的情况下,教师演示“食盐水的电解”。(或甚至教师图示讲请“食盐水的电解”的现象,总之以上均需有明晰、能观察到正确的实验现象。)
教师提问:为什么在电流通过了食盐溶液以后,阴极有氢气、阳极有氯气生成,而阴极区溶液呈碱性呢?
学生:面对这个问题,尽管学生掌握知识正确及牢固程度不同,但是都会根据这个问题活跃思维,尽量努力找出已学过的原有知识(其主要内容Ⅰ 法中已述)和新问题的内在联系。然后通过提问讨论、教师参加并随时引导以形成正确概念、原理、规律纳入知识系统。
 学生:从
H2 、Cl2 的生成可想到溶液中有 H+ 、Cl- ,联想到存在H2O
H++OH-,NaCl=Na++Cl-的电离过程,溶液中还有
Na+、OH-。比较它们的放电顺序可得出电极反应。阴极区域溶液
H+放电浓度降低影响水的电离平均移动使[OH]>[H+]呈碱性,有 NaOH
生成。
学生:从
H2 、Cl2 的生成可想到溶液中有 H+ 、Cl- ,联想到存在H2O
H++OH-,NaCl=Na++Cl-的电离过程,溶液中还有
Na+、OH-。比较它们的放电顺序可得出电极反应。阴极区域溶液
H+放电浓度降低影响水的电离平均移动使[OH]>[H+]呈碱性,有 NaOH
生成。
以上的教学从对一种食盐溶液电解的个别例子的分析,使学生完成了从
溶液中存在电解质的电离过程到确定存在离子的种类,根据放电顺序确定放电离子,得出电极反应,以及是否影响溶液的 pH 值的一般原理、规律的思考过程。明显地表现出学生整体上比Ⅱ法有更强的迁移能力。对电解 KCl、H2SO4 等溶液学生很容易分析。
教法Ⅲ与教法Ⅱ的区别在于,把在Ⅱ法中由教师随课题开展逐个提出的问题,以一个明确的、适度的、合理的综合性问题的形式全部“纳入”学生的思维中,从而深化了对学生分析、推理、归纳、综合能力的训练和培养, 提高了对学生思维品质的要求。对于学习基础好又肯积极思维的学生,他们的基础知识与思维能力得到了进一步的巩固和迅速提高;对于中等程度的学生,在讨论开展的过程中能反馈地准确填补其知识缺陷并进一步帮助他们养
成分析的习惯;对基础较差的学生能启动他们的思维机制,促使他们改变被动接受的局面。当然,对于“不投入”(即只惯于听,不试图想)的学生, 这种方法如果在一段时间里不能适应的话,会形成难以“拔起”的不利局面。
当然,对Ⅲ法的运用要求教师有深厚的专业知识功底谙熟的教学技巧, 掌握并能运用该思维规律以及教师的教学热情。但无可否定,对同样的教学内容,如果运用得当,Ⅲ法的效果最好。
从以上可以看到,在其条件基本相同的情况下,教师在进行这一同一教学内容的教学时所用的方法是可以不同的。Ⅰ法中,虽也可有简单问题插入, 如:水是强电解质还是弱电解质?它电离时生成什么离子?等等。但是学生新知识的获得是在以教师讲授为基本模式的教学过程中进行的。在教师的潜意识中存在着这种观念:知识是要教师传授给学生的,由教师“教给学生” 他们才会明白,教师讲得越清楚,学生懂得越明白。教师讲了、示范了、学生会了;没讲过、没示范过学生就不会。结果,自然是电解食盐水学生明白了,电解硫酸溶液呢?不知道。教师再从头讲吧。电解硫酸溶液会了,电解氯化铜溶液呢?又糊涂了。学生的思考在哪里呢?学生的能动性在哪里呢? 这不正是前苏联著名教育家赞科夫(190~1977 年)曾经说过:“现在的练习、练习、再练习,以及死记硬背,是几代不变的老方法。”“这种死气沉沉的守旧性,使学生失去了学习的主动性、无法教会学生创造性地思考问题或提出富有想象力的探索性的问题,后果是学生负担沉重,思想缺乏灵活性和创造性”的状况吗?这就是我们在Ⅰ法教学过程中的学生对知识迁移能力薄弱的事实中见到这种模式。
Ⅱ法、Ⅲ法与Ⅰ法的不同,区别的根本点在于Ⅱ、Ⅲ法中学生新知识的获得是在已有知识系统上,不断地通过自己的回忆、联想、比较、分类、推理、判断然后抽象概括得出结论去解决教师所提出的问题的过程中,而不是在去听懂教师所讲内容的过程中。因此学生的思维能力在教学活动进行的过程中进行着具体的训练;而教学过程的本身又在学生思维能力得到了切实提高的前提下,在解决着一个一个新问题的过程中深入开展。结果表现在学生基础知识是否已正确掌握并能加以灵活运用的知识迁移过程中。尽管Ⅱ法与Ⅲ法还有着进一步的区别,但是我们都能从中领会到美国教育家布鲁纳提倡让学生自己去探索事物发现知识并由自己去作出结论和进行概括,注意学生的理解和发现,充分发展学生的智力培养有能力的人的教育思想的可行性和重要性。
无论哪种教学方式都是由“教和学”两方面组成的,教师究竟怎样在教, 学生倒底如何学是教学过程的关键所在。如果教师把注意力更多地转向主观的教究竟是怎样作用于被其影响着的学生的学,以及客观效果又是怎样产生出来的;进一步增强以教师为主导、学生为主体的自觉意识,努力使学生在教师的启发、诱导下能动地、发现地学,使教学活动真正进行发展学生智力、提高课堂效率的过程中,那么减轻学生负担,提高教学质量是完全可以实现的。
