过程和中介
过程离不开途径,途径是过程的展开形式,过程是借助于中间环节而展开、而实现的。中间环节在哲学上称为中介,中介也就是中间环节之意。
化学过程的中介有许多具体形式,例如,过渡态、中间体等等。
过渡态概念是 20 世纪 30 年代提出来的。珀兰尼(Polanyi)称之为过渡态,艾琳(Eyring)称之为活化络合物。过渡态是一种极不稳定的络合物, 它是从反应物到产物的中间环节。现在,过渡态概念也被引入哲学,成为哲学研究的一个概念。
化学中的过渡态,不仅是一个中介,而且是控制环节。因为作为过渡态的活化络合物分解才能得到产物,使化学过程完成,而活化络合物分解为产物这一步,是控制反应速度的决定性的一步,它的速度决定了整个过程的速度。
化学过程的中介,除了过渡态外,还有其他许多形式。例如,有机反应中的活性中间体:自由基、离子基、正碳离子,催化理论中的中间化合物、催化活化过渡态,等等,都是过程的中介,借助于这些中介的具体形式,使过程由此达彼,使反应物转化为产物。
下面,对这些作为中介的不同形式作一简要说明。
自由基,也叫游离基,具有不成对电子的原子、分子或基团等。基的概念产生很早,据肖莱马(Carl Schorlemmer)考证①,最先应用基(labase) 或根(Le radical)这些术语的是拉瓦锡的友人德莫武(Guyton de Morveau), 而拉瓦锡本人则把化合物中和氧结合的部分叫做基或根。后来,在有机化合物的基团理论中,基被视为有机化合物中不发生变化的基团,它的作用犹如无机化合物中的元素。这个理论使化学家提出了制备游离基(即自由基)的任务。19 世纪 40~60 年代,弗兰克兰、柯尔柏、布特列洛夫等人分别用不
① 肖莱马:《有机化学的产生和发展》,潘吉星译,科学出版社,1978 年版,第 11~12 页。
同方法试图得到自由基,但都没有成功。直到 1900 年,冈伯格才发现碳自由基,得到了三苯甲基自由基的黄色溶液;1929 年,潘内斯等人又测定了甲基和乙基的生成。本世纪 30 年代,海伊、沃特斯、卡拉什等人研究发现,有机自由基可作为活泼中间体形成链反应。
离子基,是带电荷的正、负离子自由基,正如前面指出过的,它兼有离子和自由基的特点,既带电荷又有不成对电子。离子是 19 世纪发现的。从1832 年开始,法拉第进行电解实验,1833 年发现了电解定律,1834 年为解释电解现象,将溶液中被电解出来的带电荷的物质称为离子,1887 年,阿伦尼乌斯提出,电解质在水中离解成离子。20 世纪,发现电子和建立原子结构模型以后,离子的形成机理得到了解释。在发现自由基并确立自由基的结构以后,将离子和自由基结合起来,形成了离子基概念。离子基可以发生自由基型反应、离子型反应和电子转移反应。
正碳离子,是带有正电荷的含碳离子。20 世纪 20 年代,英戈尔德等人研究有机化学反应机理时提出了正碳离子及其反应,正碳离子被认为是共价C—C 单键中一对电子的异裂反应而产生的,它是一类重要的活性中间体。
除上述的以外,还有温斯坦提出的非经典正碳离子(它是具有某些结构特征的正碳离子),负碳离子,卡宾(又称碳烯),等等。所有这些都是活性中间体的不同形式。化学家们经研究发现,有机化学反应如同其他类型的反应一样,都要经过一定的步骤,或者叫做历程。按照传统的分类,反应历程分为两类:离子反应历程和自由基反应历程。20 世纪 20 年代发现了双烯加成反应,它既不属于离子反应历程也不属于自由基反应历程,曾被称为“无历程反应”。多数有机反应是有历程反应。“无历程反应”是相对于过去已知的有历程反应而言的,“无历程反应”是一步反应,也有一个过渡态。有历程反应,或者说阶段反应从反应物到产物,中间形成活性中间体,它寿命很短,非常活泼,是从反应物到产物的中介。
化学中对催化过程的解释产生了各种理论。中间化合物理论认为,在催化反应中,催化剂先与某一反应物发生作用,生成活性中间化合物,此中间化合物进一步反应生成产物,同时催化剂分解出来。在此过程中,中间化合物就起了中介作用。催化活化过渡态理论则认为,在催化反应中,反应物分子与催化剂表面的活性中心形成吸附活化络合物,进一步反应转变为产物。在此过程中,吸附活化络合物也具有中介作用。在此基础上进一步发展起来的多位催化理论、多位集团催化理论等,虽然对催化反应机理的解释有所不同,但是其基本思想中有共同点,这就是存在着过渡和中介。
广义地说,化学反应都有其从反应物到产物的具体途径,或叫做历程。化学反应所经历的具体途径,都具有中介的性质,它们都是由此达彼的桥梁, 或者说,都是从反应物到产物所经历的中间环节。
通常的化学计量反应方程式,如 H2+Br2=2HBr 反映的是化学反应的总过程、总结果和计量关系。这种反应式所表示的是总反应,是宏观化学反应过程。一个总反应是由一个或数个基元反应构成的,所谓基元反应是指反应物微粒一步直接转化为产物微粒的过程,每一基元反应又是由许许多多的微观上的分子变化所构成的,微观上的分子变化叫做基元分子过程。
两个或两个以上的基元反应集合起来构成复合反应,构成复合反应的基元反应的集合,称为反应历程,也就是反应物转化为产物所经历的途径与步骤。从揭示反应历程的角度看,复合反应过程可以分成几种形式:连串反应
过程、平行反应过程、对峙反应过程和链反应过程。
连串反应或连续反应是前后相继的几个基元反应构成的复合反应。所谓前后相继,指的是前一基元反应的产物恰是后一基元反应的反应物,可以下式表示:
A→B→C→D⋯⋯
放射性衰变过程是一种连续反应过程,例如:
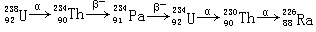
诚然,这种放射性衰变过程是一种核反应,不是一般的化学反应,核反应是核化学研究的内容。一般化学反应中也存在连续反应形式,例如,邻二甲苯的液相氧化,如下所示:
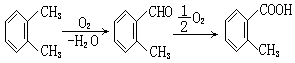
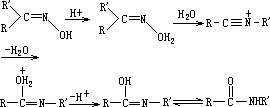 有机化学中的重排反应,是有机化合物分子中共价键结合顺序发生改变的反应,从实质上看也具有连续反应的性质。例如,德国化学家贝克曼于
1886 年发现的酮肟在酸性条件下发生重排生成
N-烃基酰胺的反应,反应过程如下式所示:
有机化学中的重排反应,是有机化合物分子中共价键结合顺序发生改变的反应,从实质上看也具有连续反应的性质。例如,德国化学家贝克曼于
1886 年发现的酮肟在酸性条件下发生重排生成
N-烃基酰胺的反应,反应过程如下式所示:
从上式可以看出,这个反应具有前后相继的形式。
 平行反应是反应物同时参加两个或两个以上的基元反应所构成的过程,
具有如下式所示的形式:
平行反应是反应物同时参加两个或两个以上的基元反应所构成的过程,
具有如下式所示的形式:
例如,乙醇可以进行脱水反应也可以进行脱氢反应。
对峙反应又叫可逆反应,由一个正向的基元反应和逆向的基元反应构成,正向反应的产物恰好是逆向反应的反应物。
链反应是一类重要化学反应,由于反应过程中活性中间体(如自由基或自由原子)的交替和重复产生,使反应物分子转变为产物分子。在反应体系中,依靠光、热、化学引发,使稳定分子分解为自由基,一旦引发,反应会持续进行下去,旧链载体消失新链载体产生,直到链载体消亡,使链反应终止。例如:
H2+Cl2→2HCl
开始为光引发,即 Cl2+hv—→2Cl 随之发生反应: Cl+H2→H+HCl
H+Cl2→Cl+HCl
以上说明,任何一个化学总反应过程都是从反应物转化为产物的过程, 可写成:
反应物(总)→产物(总)
任何一个基元反应也是从反应物转化为产物的过程,可写成:
反应物→产物每一基元反应只有一个“反应物→产物”,而每一个“反应物→产物”都是总反应中经历的一个步骤。例如,在 H2+Br2→2HBr 的反应中,历程为:
Br2→2Br
Br+H2→HBr+H H+Br2→HBr+Br H+HBr→H2+Br 2Br—→Br2
其中每一个“→”都表示一个基元反应,即反应物转化为产物,该基元反应的产物又成为后一基元反应的反应物,依此类推。在连续反应、对峙反应和平行反应中,情况也都如此。总之,“反应物(元)产物(元)”乃是化学过程的基本构成要素、基本环节,或者说是构成化学过程的“细胞”。
反应物和产物都是物,在宏观上表现为实物,在微观上表现为微粒,可以是分子、原子和离子,也可以是原子团、自由基,它们具有实体性,或者说它们都是化学实体。在这个意义上说,它们是物而不是过程。可是由物形成的关系,即“反应物→产物”,已经是过程。化学过程是由物的关系、由“反应物—→产物(元)”的总和构成,而“反应物(元)→产物(元)”则是过程的载体。在这里已表现出实体、关系和过程三者之间是有联系的。下面, 让我们进一步分析这种联系,并讨论与此有关系的一些哲学问题。
