化学变化的形式和内容
化学变化在化学中叫化学反应。化学反应有多种多样的形式,如分解反应、化合反应、氧化—还原反应、酸碱中和反应、缩合反应、取代反应、加成反应、重排反应等等,它们都是某种粒子的转移过程。从粒子转移过程的角度,可以把化学反应分成如下几种类型:
电子转移反应,即原子的氧化数变化产生的氧化—还原反应。氧化—还原反应总是伴随着电子从一个原子向另一个原子的转移过程。依据电子理论,得电子者叫氧化剂,失电子者叫还原剂,氧化—还原反应是在氧化剂和还原剂相互作用中发生的反应。氧化—还原反应可以再细分成两类:分子(或原子)间的氧化—还原反应和分子内的氧化—还原反应。分子(或原子)间的氧化—还原反应,是在不同分子或原子之间发生的,例如:
2Na+Cl2=2NaCl
2HgCl2+[SnCl4]2-=Hg2Cl2+[SnCl6]2-
分子内的氧化—还原反应,是在分子内原子之间发生的,例如: ZrI4=Zr+2I2
NH4NO3=N2O+2H2O 4KClO3=3KClO3+KCl
氧化—还原反应的发生,取决于原子之间、分子之间或分子内部原子之间电子的转移,这种氧化—还原反应属于电化学氧化—还原反应。
电子对转移反应,也可以叫做配体交换反应。在反应中,电子对从电子给体向电子受体作不完全的转移,形成配位键。
质子转移反应,即酸碱中和反应。依据质子理论,酸是交出质子的物质, 碱是接受质子的物质,酸和碱形成共轭关系,如下式所示:
 CH3COOH+OH-
CH3COO-+H2O
CH3COOH+OH-
CH3COO-+H2O
酸 碱 碱 酸
原子分子粒子转移反应,如原子分子置换、同位素置换、自由基置换、有机化合物分子及其他分子中亲电子和亲核交换等,这类反应的发生导致一些原子分子粒子被另一些原子分子粒子所替换。例如:

 H2SO4+D2O
HDSO4+HDO C6H6+HONO2→H2O+C6H5NO2 CH3Br+HOH CH3OH+HBr
H2SO4+D2O
HDSO4+HDO C6H6+HONO2→H2O+C6H5NO2 CH3Br+HOH CH3OH+HBr
⋯⋯
这些反应的特点在于,反应中在相当程度上保持了被转移的原子分子粒子的性质。离解作用、缔合作用、聚集作用也是原子分子粒子的转移过程。离解作用,包括
①分子离解为原子,例如,
hv
Br2 → 2Br;
②分子离解为离子,例如: I2→I++I-;
③热解聚或光化学解聚,例如,
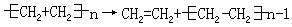
缔合反应是离解反应的逆反应,例如, CH3·+NO2·→CH3NO2 CH3COOH+CH3COOH→(CH3COOH)2
⋯⋯
聚集作用是由原子分子粒子和缔合体形成的聚集体。
有机化合物和高分子化合物,数量多,结构复杂,这就决定了有机化学反应和高分子反应的具体形式具有极其多样性的特点。从化学键断裂方式看,可分成两类:一类是在反应之中成键的一对电子平均分给两个原子或原子团,另一类是成键的一对电子为某一原子或原子团所占有,前者为自由基型反应,后者为离子型反应。离子型反应又可分为亲电反应和亲核反应。如此等等。
仅从上面的简单描述中可以得出结论,化学反应的形式是多种多样的; 但是,它们具有共同的内容,这就是电子、质子、原子分子粒子的转移。内容(或本质)通过形式(化学反应的具体形式)表现出来,形式反映内容。因此,化学反应形式与某种粒子的转移之间的关系,是形式和内容的关系。化学从研究化学反应入手,揭示其内容,通过对化学反应内容的认识,又帮助对具体化学反应的研究,指导这种研究。
通过各种各样的化学变化,自然界中的物质复杂化了、向前发展了,这就涉及化学进化了。下面讨论化学进化问题。
