碱的通性酸碱度的表示方法——pH 值
碱的通性从以上的学习中,可以看出碱类有许多相似的性质,主要有以下几点。
- 碱溶液跟酸碱指示剂的反应
碱的水溶液能跟酸碱指示剂反应而使指示剂呈现一定的颜色,如使石蕊试液呈蓝色,使酚酞试液呈红色等。
- 碱跟某些非金属氧化物(酸性氧化物)的反应碱跟酸性氧化物反应生成盐和水,例如:
Ca(OH)2+CO2====CaCO3↓+H2O 2NaOH+SO3===Na2SO4+H2O
碱跟酸性氧化物反应的文字表达式为:
碱+酸性氧化物→盐+水
非金属氧化物大多数是酸性氧化物。许多酸性氧化物能溶于水,跟水化合生成酸。例如:
CO2+H2O====H2CO3 SO3+H2O===H2SO4
- 碱和酸的反应
碱能和酸发生中和反应,生在盐和水即碱+酸→盐+水
【实验与思考】
把盐酸滴入盛有少量氢氧化铁的试管,观察现象。这一反应的化学方程式是:
Fe(OH)3+3HCl====FeCl3+3H2O
- 碱跟某些盐的反应
碱溶液能跟某些盐溶液起反应,生成另一种碱和另一种盐。即: 碱+盐→新碱+新盐
例如: 3KOH+FeCl3====Fe(OH)3↓+3KCl
以上碱类的四条通性,不仅表明了碱具有能跟酸性氧化物、酸、盐等类物质反应的性质,同时也反映了碱与其它各类物质之间的关系。这种关系可以用图 9-11 来表示。
碱类物质之所以具有一些相似的性质,是由于碱类在水溶液里电离生成
的阴离子都是氢氧根离子的缘故。碱的命名
碱是根据它的组成——氢氧根离子和金属离子的名称,命名为“氢氧化某”。如 Mg(OH)2 叫做氢氧化镁,Cu(OH)2 叫做氢氧化铜等等。如果某种金属能形成带不同数量电荷的离子时,一般把具有高价金属离子的碱叫做“氢氧化某”,把具有低价金属离子的碱叫做“氢氧化亚某”,如 Fe(OH)3 叫做氢氧化铁,Fe(OH)2 叫做氢氧化亚铁等等。
【家庭小实验】1.自制叶脉书签
向少量稀氢氧化钠溶液(或适量新制的熟石灰和纯碱混和加水煮沸所得的悬浊液)中,投入几片树叶并使树叶浸泡在溶液中,煮沸 6~10 分钟。取出树叶放在清水里洗去碱液,再用毛刷轻轻刷去叶肉,将叶脉晾至半干后着上你喜欢的颜色。晾干后一张漂亮的叶脉书签就做成了。
2.自制皮蛋
按以下配方和步骤自制 4 只无泥皮蛋。
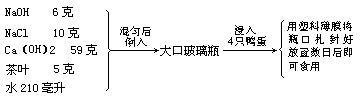
pH 值——酸碱度的表示法酸或碱能使指示剂变色,这是酸碱的重要化学性质。利用这条性质,可以根据指示剂在溶液中的颜色来确定溶液的酸碱性。但在实际生活中,仅仅知道某种溶液是酸性还是碱性是很不够的,还必须测定和控制溶液的酸、碱性强弱程度,即溶液的酸碱度。溶液的酸碱度常用 pH 值表示,pH 值的范围通常在 0~14 间(图 9-12)。
pH 值等于 7 时,溶液呈中性,pH 值小于 7 时,溶液呈酸性,pH 值越小, 溶液的酸性越强;pH 值大于 7 时,溶液呈碱性,pH 值越大,溶液的碱性越强。
【思考与练习】
图 9-13 是人体内几种体液或代谢产物的正常 pH 值,其中哪些偏酸性, 哪些偏碱性,哪一种酸性最强,哪一种碱性最强?
pH 值的测试
测定溶液的 pH 值有多种方法,可以根据检测要
求的精确度选用不同的方法,如果要求精确些,可以用酸度计(图 9-14) 等仪器。简单的方法通常是使用 pH 试纸。pH 试纸是浸渍过多种酸碱指示剂的试纸。这种试纸在不同酸碱度的溶液里,显示不同的颜色。测定时,把待测溶液滴在 pH 试纸上,然后把试纸显示的颜色跟标准比色卡对照,便可知道溶液的大致 pH 值。
【实验与思考】
取一小撮菜叶、少许土壤、一小块水果,分别捣烂,各放到一支试管里, 分别加入蒸馏水 3 毫升。用玻璃棒搅拌,静置。把三条 pH 试纸分开放在玻璃片上,分别用玻璃棒蘸取菜叶、土壤、水果的浸出液滴在 pH 试纸上,测定三
种浸出液的 pH 值。并把测定结果按酸性由强到弱或碱性由弱到强的顺序排列。
【实验与思考】
向一只烧杯中加入水 120 毫升、浓盐酸 1 毫升,搅匀后用 pH 试纸进行测试。然后从此烧杯中取出 1 毫升溶液,倒入另一只洁净的烧杯里,加水稀释
到 100 毫升再进行测试。比较两次测试结果。
测定溶液的 pH 值在生产实际中具有重大意义,因为化工生产中的化学反应要在适当的 pH 值范围内才能正常进行。大多数农作物最适宜在中性或接近中性的土壤里生长,当土壤的 pH 值小于 4 或大于 8.5 时,一般农作物就难以生长,一些农作物最适宜生长的 pH 值范围如表 9-2。
