总复习题
- 填空
-
盛放石灰水的瓶中常形成一层不溶于水的白色固体,它是 ,化学式为 ;用 可以将这种固体除去,主要反应的化学方程式为 。
-
胆矾晶体中结晶水的质量百分含量为 ,把 25 克胆矾溶于 75 克水中所得溶液的质量百分比浓度为 。
-
有甲、乙两组试剂,甲组:Na2CO3、HCl、CuSO4;乙组:Ca(OH)
2、BaCl2、Fe。其中甲组中的能与乙组中的所有物质反应,乙组中的 能
与甲组中的所有物质反应。
-
使一杯接近饱和的硝酸钾溶液转化为饱和溶液,可用 、 、 三种方法。
-
用简易装置制备氢气的主要操作步骤有:①加入锌粒,注入盐酸;
②连接装置;③检查装置气密性;④塞上带导管的橡皮塞;⑤检验氢气的纯度;⑥固定在铁架台上;⑦收集氢气准备做性质实验。其正确的操作顺序应为 (填序号)。
- 向 40 克 10%的 NaOH 溶液中加入 60 克 20%的 NaOH 溶液,混和后,溶液的质量百分比浓度为 ,pH 值 7(填大于、等于或小于);上述混合溶液,恰好能跟 克 10%的稀 HCl 完全反应,反应后溶液中的溶质是
,溶液的质量百分比浓度为 ,pH 值 7(填大于、等于或小于)。
(7)20℃时,将 15.8 克硝酸钾加到 50 克水中配成饱和溶液,则该溶液的质量百分比浓度为 ,20℃时硝酸钾的溶解度为 。若将上述溶液稀释到 100 克,此时溶液的质量百分比浓度为 。
- 下表括号内为混合物中含有的少量杂质,分别写出除去杂质应选用的试剂及有关的化学方程式。
|
混合物 |
选用试剂 |
反应的化学方程式 |
|---|---|---|
|
HNO3 ( HCl ) |
||
|
NaOH ( Na2CO3 ) |
||
|
SiO2 ( Fe2O3 ) |
- 有 A、B、C 三种物质,已知 A 为钠盐、B 为氯化物、C 为碱。经下列实验操作,其结果分别是:
①A、B 的溶液混和后无沉淀或气体产生;
②B、C 的溶液混和后出现蓝色沉淀;
③A、C 的溶液混和后出现白色沉淀,该沉淀不溶于稀硝酸。则可能 A 为 ,B 为 ,C 为 (填化学式)
- 从 Zn、BaCl2、Fe(OH)3、NaOH、KClO3、CuCl2、Na2SO4、CaO、H2O、H2SO4 等物质中,选出适当的物质,按下列要求写出化学方程式:
①化合反应
②分解反应
③置换反应
④复分解反应:a (酸与盐反应) b (碱与盐反应) c (盐与盐反应)
- A、B、C 分别代表一种纯净物,试根据下面实验所得出的它们的转变关系,推断它们各为什么。
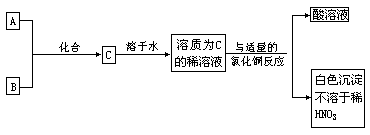
则可能 A 是 或 ,B 是 或 ,C 是 ,最后一步转变的化学方程式是 。
- 选择题(每题只有一个选项符合题意,请将所选项的序号填在题后的括号里)
- 下列变化中,属于化学变化的是 [ ] A.白磷自燃
B.分离液化空气制氧气 C.干冰变成二氧化碳气体
D.在晾干的咸菜表面出现食盐晶体
-
不宜用排空气集气法收集的气体是 [ ] A.H2 B.O2 C.CO2 D.CO
-
遇火不可能发生爆炸的混合物是 [ ] A.氢气和空气 B.水煤气和空气
C.散布有面粉尘的空气 D.二氧化碳和空气
- 区别 CO 和 H2,可用的方法是 [ ]
A.通到水中观察溶解性的大小 B.将燃烧产物通入石灰水观察现象C.点燃后观察火焰颜色 D.观察与灼热的氧化铜是否反应
-
只用一种试剂来鉴别 NaOH、Ca(OH)2、稀 H2SO4 三种溶液,这种试剂是 [
]
- 氯化钡溶液 B.紫色石蕊试液
C.碳酸钠溶液 D.无色酚酞试液
-
下列物质在盛有氧气的集气瓶中燃烧后,瓶壁有水雾出现,注入少量石灰水,振荡后出现浑浊的是
[ ]
- 一氧化碳 B.氢气
C.木炭 D.甲烷
-
下列反应中,没有沉淀产生的是 [ ]
- 氯化氢气体通入硝酸银溶液B.二氧化碳通入氯化钙溶液
C.氯化钡溶液中加入三氧化硫
- 氯化氢气体通入硝酸银溶液B.二氧化碳通入氯化钙溶液
D.二氧化硫通入过量的饱和石灰水中
- 分别将少量下列各组物质同时加到足量水中,得到无色透明的混合
|
溶液的是 |
[ |
] |
|---|---|---|
|
A.FeCl3、KOH、NaCl C.CuSO4、HCl、KCl |
B.K2SO4、BaCl2、HCl D.Na2CO3、KCl、Na2SO4 |
- 在 CuCl2 和 MgCl2 的混合溶液中加入过量的锌粉,充分反应后过滤,
|
留在滤纸上的物质是 |
[ ] |
||
|---|---|---|---|
|
A.Zn |
B.Cu |
C.Cu 和 Mg |
D.Zn 和 Cu |
- 实验室里制取氧气大致可分为下列步骤:a.点燃酒精灯,加热试管;b.检查装置的气密性;c.将高锰酸钾装入试管,用带导管的塞子塞紧试管,并把它固定在铁架台上;d.用排水法收集氧气;e.熄灭酒精灯;f.将导气管从水槽中取出。
|
正确的操作顺序是: |
[ |
] |
|---|---|---|
|
A.b—c—a—d—e—f |
B.c—b—a—d—e—f | |
|
C.b—c—a—d—f—e |
D.c—b—a—d—f—e |
- 有 X、Y、Z 三种金属,将 X 和 Y 浸入稀硫酸中,Y 溶解,X 不溶解;将 X
浸入 Z 的硫酸盐溶液,在 X 的表面有 Z 析出。则 X、Y、Z 的金属活动性按由强到弱的顺序为 [ ]
A.Z、Y、X B.Y、Z、X
C.Z、X、Y D.Y、X、Z
- 有 50 克 5%的 NaCl 溶液,若将其浓度增加一倍,应采用的方法是 [ ]
A.把溶剂蒸发掉一半 B.加入 2.5 克 NaCl 固体
C.把溶剂蒸发掉 25 克 D.加入 50 克 5%的 NaCl 溶液
-
甲元素原子与乙元素原子的质量比为 a∶b;而乙元素原子与碳- 12
原子的质量比为 c∶d,则甲元素的原子量为 [ ]
-
bc 12ac
-
2ac
-
bd
- 2bd
ac
- ad 12bc
- 在氢气还原氧化铜的实验中,如果反应生成 12
克水,那么剩余固体的质量比原来氧化铜的质量约减少 [ ]
A.10.7 克 B.12.3 克 C.16.2 克 D.22.1 克
(15)X 和 Y 两种元素可以组成两种化合物 A 和 B,A 中含 X 的质量百分数为 50%,B 中含 X 的质量百分数为 40%,若已知 A 的化学式为 XY2,则 B 的化学式为 [ ]
- XY B.X2Y C.XY3 D.XY4
(16)50℃时的某饱和溶液冷却至室温后,析出少量无水晶体,下列说法中不正确的是 [ ]
A.溶剂的质量没有改变B.留下的溶液仍然饱和C.溶液中溶质质量改变D.溶液的浓度保持不变
-
固态物质 a 与盐酸反应生成溶液 c,c 与 NaOH 溶液反应得到沉淀b,b 加热又转变为 a,则 a 是下列物质中的 [ ]
- Fe(OH)3 B.Mg C.Na2O D.CuO
-
一块质量为 6.5 克的不纯锌块中,可能含有下面一种金属,当该
锌块与足量的稀硫酸完全反应后,得到氢气 0.19 克,则锌块中可能含有的金属是 [ ]
- Cu B.Fe C.Mg D.Al
- 有 a 克硝酸钾溶液,质量百分比浓度为 25%,若要使其浓度变为
|
50%,可选择的方法是 ①加入硝酸钾 0.5a 克 |
②加入硝酸钾 0.25a 克 |
[ |
] |
|---|---|---|---|
|
③蒸发掉 0.5a 克溶剂 A.②③ B.①④ |
④蒸发掉 0.4a 克溶剂 C.①③ D.②④ |
- 只用①Fe2(SO4)3②Na2CO3③AgNO3④石蕊试液中的一种,就能将BaCl2、HCl、NaOH 三种无色溶液一次鉴别出来的有
[ ]
A.①② B.①②④ C.①②③ D.①③④
-
失去标签的四瓶无色溶液,只知它们是盐酸、碳酸钠、氯化钙、硝酸钾,取标有 A、B、C、D 的四支试管,分别加入四种溶液各少许,将 A 试管中的溶液分别加到其它三支试管中,B 试管中出现白色浑浊,C、D 试管中无现象,则可判断 A 试管内原溶液是 [ ]
- 盐酸 B.碳酸钠 C.氯化钙 D.硝酸钾
-
已知一种碳原子(质子数、中子数均为 6)的质量为 m 克,铁的原子量为 n,则一个铁原子的质量约为 [ ]
- 12 克
mn
- 2m 克
n
- mn 克
12
- n 克
12m
- 下列说法中,不正确的是 [ ]
A.金属活动性顺序表中氢前面的金属能置换出酸中的氢
- 催化剂不一定都能加快反应速度C.金属氧化物不都是碱性氧化物
D.冷却饱和溶液,必有晶体析出
- 有浓度为 5%的 MgSO4 溶液 240 克,若蒸发掉 215.4 克水,剩下的水刚好与溶质形成 MgSO2·xH2O,此 x 的值为 [ ]
A.7 B.6 C.5 D.3
- 在下列溶液中加入铁粉,溶液质量增加的是
[ ]
- 硫酸铜 B.硝酸银 C.硫酸钠 D.稀硫酸3.简答题
如下图所示实验,已知 A 为 H2、CO 中的一种或两种的混合物,甲装置中的黑色粉末为氧化铜、炭粉中的一种或两种的混合物,根据下列要求回答:
- 若黑色粉末是纯净物,甲、乙、丙三装置依次出现红色、蓝色、浑
浊,则 A 气体是 ,黑色粉末是 。
-
若 A 为纯净物,反应现象同题(1),则 A 气体是 ,黑色粉末是 。
-
若题(1)乙装置中物质增重 3.6 克,丙装置中物质增重 4.4 克,
则至少要通入 A 气体 克。
- 若题(2)甲装置生成红色物质 6.4 克,乙装置中物质增重 O.9 克,
则黑色粉末的质量至少要 克。4.实验题
- 将下列实验报告的空白处填写完整。
|
样品序号 |
实验步骤 |
实验现象 |
结论 |
|---|---|---|---|
|
( 1 )取少量溶液滴加氢氧化钠 |
( 1 ) |
||
|
溶液。 |
|||
|
溶液 A |
( 2 )过滤,将滤渣转移到坩埚 |
( 2 ) |
A 是 Fe2(SO4)3 溶液 |
|
中,加热 |
|||
|
( 3 )滤液中滴加BaCl2 和稀HNO3 |
( 3 ) |
||
|
溶液 B |
( 1 ) ( 2 ) |
( 1 )溶液 B 变浑浊 ( 2 )无色溶液变红色 |
B 是 Ca(OH)2 溶液 |
|
( 1 )取少量溶液加入少量 锌 |
( 1 )有大量气泡产生, |
||
|
粒。 |
锌粒溶解 |
||
|
溶液 C |
( 2 )取少量溶液滴加紫色 石 |
( 2 )溶液变为红色 |
C 是 |
|
蕊试液。 ( 3 )取少量溶液滴加 AgNO3 溶 |
( 3 )有白色沉淀生成, |
||
|
液和稀 HNO3 |
该沉淀不溶于稀硝酸 |
- 为除去硝酸钾中混有的少量氯化钙和氯化钠,设计了如下实验方案。请在括号中填上适当的试剂,在横线上用化学式表示有关物质,写出有关反应的化学方程式。
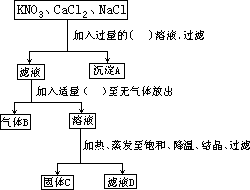
A ,B ,C ,D 和 。有关反应的化学方程式:
生成沉淀 A 生成气体 B 5.计算题
把表面已氧化的镁条 5.2 克放入盛有足量盐酸的烧杯中,充分反应后称
量,溶液的质量比原来表面已氧化的镁条与盐酸的质量总和减少 0.4 克。求:①镁条中氧化镁的质量百分含量。
②氧化前镁的质量为多少克?
