1990 年复赛试题
(时限 150 分;满分 100 分)
注意:1)答卷可用计算器;
2) 原子量: S(32.06) Ru(101.1) H(1.008) O(16.00) Fe(55.85)
一、(本题 6 分)
400℃下,1dm3 容器内 N2 、H2 、NH3 三种气体的平衡浓度分别是: [N2]=1.0mol·dm−3, [H2]=0.50mol·dm−3,[NH3]=0.50mol·dm−3。如果保持温度不变,而要使 N2 的平衡浓度增加到 1.1mol·dm−3,需从容器中取走多少摩尔的氢气才能使体系重新达到平衡?
二、(本题 10 分)
足量的硫酸铁溶液在煮沸条件下被 25.00cm3 的 0.0494mol·dm−3 羟胺(NH2OH)酸性溶液还原为亚铁离子。生成的亚铁离子可与 24.65cm3 的高锰酸钾溶液作用完全。若用上述高锰酸钾溶液滴定 25.00cm3 0.0500mol · dm−3 的硫酸酸化的草酸钠溶液,则耗高锰酸钾溶液
24.80cm3。
由上述事实,推导 NH2OH 被硫酸铁氧化的产物,并写出二者反应的方程式。
三、(本题 20 分)
钌(Ru)的硫化物可用元素合成法(下称干法)和湿法获得。干法用99.9%的纯钌粉和 99.99%的硫按化学计量配料,充分混合,置于石英管中,抽真空并加热至 800℃反应生成,经 X−射线检定为晶态。湿法:可在六氟合钉(IV)
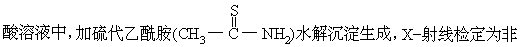
晶态。制得的两种硫化物,在较高温度下用氢气还原,生成的 H2S 利用库仑滴定法进行测定,可计算出硫量,还原后得到的金属钌进行称量测定。两种方法制得的硫化物在空气中都有微吸湿性,利用失重法可计算出化合物的含水量。其实验数据如下:
| 试样组成 | S |
Ru |
H O 2 |
|---|---|---|---|
| (1)干法 |
37.26 % |
60.06 % |
2.73 % |
| (2)湿法 |
20.63 % |
41.84 % |
37.36 % |
-
试推断干法和湿法制得的两种硫化物的化学式。
-
写出湿法制备硫化物的反应方程式(要求配平)。
-
哪种方法制得的硫化物测定结果偏高?导致结果偏高的原因可能是什么?
-
用氢还原钌的硫化物,每升温 20℃,保温 5
分钟,同时库仑滴定这一期间释放的 H2S 量,直到无 H2S 逸出,化合物还原为金属钌为止。若以滴定 S2−离子的时间(s)为纵坐标,温度(℃)为横坐标作图,得钌硫化物被氢还原的反应速率相对于温度的动力学曲线,如下图:
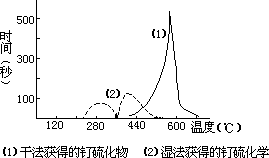
据此,比较两种硫化物对氢作用的稳定性 5.图中湿法制得的硫化物有两个脱硫峰,而且由第一个峰测得的硫
1
含量大约为化合物含硫总量的 3 。据此,推测氢还原湿法制得的钌硫
化物的过程。
6.图中(2)的第二个脱硫峰的温度区间比(1)脱硫峰要低,其可能原因是什么?
四、(本题共 15 分)
组成晶体的最小重复单位称为晶胞。氯化钠晶体的晶胞是大家熟知的:它是一个立方体,在立方体的体心和立方体的每条棱边的中点各有一个 Na+(或 Cl−),在立方体的每一个角顶和每个面心各有一个 Cl−(或Na+)。已知一种铁的氧化物 FexO(富氏体)为氯化钠型结构,由于存在缺限 x<1,测得其密度为 5.71g·cm−3。用 MoKa 射线(λ=71.07pm)测得其晶胞边长为 428pm(1pm=10−12m)。
-
算出 FexO 中的 x 值;
-
FexO 中 Fe(Ⅱ)和 Fe(Ⅲ)各占总铁量的百分之几?
(3)写出标明铁的价态的该晶体化学式;
-
在 FexO 晶体中,O2−的堆积方式是立方密堆积、六方密堆积,还是简单立方堆积?Fe 在此种堆积中占据哪一类空隙?占有分数是多少?
-
FexO 晶体中 Fe—Fe 之间的最短距离是多少 pm?
五、(本题共 19 分)
同位素有稳定同位素和放射性同位素之分。前者不具有放射性,如206Pb,87Sr 等;后者能自发地放射出射线,如 87Rb 放射出β射线,238 U 经一系列α和β射线放射,最终衰变为 206Pb。
- 写出下列衰变反应:
-
87Rb 的β−衰变反应式 ;
-
从 238 U 到 206Pb 衰变的总反应式 。
2.放射性衰变是一级反应,其速率方程满足下式: N=Noe−λt
式中 No 为开始时放射性核的数目,N 为 t 时间时放射性核的数目,λ称
为衰变常数。放射性核有半数发生衰变需要的时间称为半衰期,以t 1 表
2
示。如上述核反应(1)的t = 5.7×1010 年,核反应(2) 的t = 4.5×109 年。
2 2
某些放射性同位素的功能就像一座“天然钟”,协助人们记录古代某些岩石沉积物固化的时间。如从月球表面取回的岩石试样,经分析获得下列摩尔比:
87Sr/87Rb=0.041,206Pb/238U=0.66
用上列数据,求此岩石试样的年龄。 3.对这种估算岩石年龄的方法进行评价。六、(本题共 18 分)
“蜂皇质”可经下列反应合成来推导它的结构。一个酮 A(C7H12O)与CH3MgI 作用后水解生成一个醇 B(C8H16O)。B 脱水后生成烯 C(C8H14)。C 臭氧氧化还原水解仅得一个化合物 D(C8H14O2)。D 在碱存在下,与丙二酸二乙酯反应得到的产物在热酸中水解得到“蜂皇质”E(C10H16O3)。E 经催化加一摩氢生成酮酸F(C10H18O3)。F 与I2+NaOH 反应(碘仿反应)生成CHI3 和壬二酸。请写出 A、B、C、D、E 和 F 的结构。
A: B: C: D: E: F: 七、(本题共 12 分)
化合物 A(C10H16)是存在于桔子、柠檬及柚子皮中的一个烯烃。A 吸收两摩的氢形成烷烃 B(C10H20)。A 被高锰酸钾酸性溶液氧化成化合物 C:
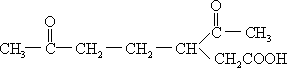
A 在催化剂作用下加两摩水,生成一个无手性的醇类 D。试问: 1.化合物 A 的结构中有无环?如有的话,有几个环?
-
哪些结构可能氧化成 C?
-
写出 D 的结构。
4.A 最可能是哪种结构?
5.B 最可能是哪种结构?
