四、由实验事实判断未知物
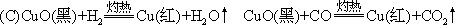

 1.(a)HCl、SO2、CO、H2
(b)Br2+SO2+2H2O 2HBr+H2SO4 Ba(NO3)2+H2SO4 BaSO4↓(白)+2HNO3
1.(a)HCl、SO2、CO、H2
(b)Br2+SO2+2H2O 2HBr+H2SO4 Ba(NO3)2+H2SO4 BaSO4↓(白)+2HNO3
2.(a)AlCl3,NaHCO3 (b)3NaHCO3+AlCl3 3NaCl+Al(OH)3↓+3CO2

 ↑NaAlO2+CO2+2H2O
Al(OH)3↓+NaHCO3
↑NaAlO2+CO2+2H2O
Al(OH)3↓+NaHCO3
- 该化合物中碳、氢、氧原子个数之比为:
63.1 ∶ 5.30 ∶ 31.6 = 5.26∶5.25∶1.98 = 2.66∶2.65∶1.00 = 5.32∶5.30∶2.00
12.0 1.01 16.0
=7.98∶7.95∶3.00 至此,最后边三个数均可看成整数,因为它们与整数相差的尾数都在提供的数据的实验误差范围内,可用四舍五入得整数, 因此最简式为 C8H8O3。
 五、(1)求碘溶液浓度I2+2S2O32−
2I−+S4O62−
五、(1)求碘溶液浓度I2+2S2O32−
2I−+S4O62−
22.5 × 0.100 = 0.0450mol·L−1
2 × 25.0
- 求稀释后 SO2 水溶液浓度
SO + I + 2H O === SO2− + 2I− + 4H +
(25.0 × 0.045 − 9.30 × 0.100 / 2) × 1 = 0.0660mol·L−1
1 × 10.0
- 求原始 SO2 水溶液的浓度
0.0660 × 500 = 3.30mol·L−1
10.0
- 求 S2Cl2 与 SO2 反应的物质的量之比,并书写反应式。
n ∶n =( 1.68 × 10.0 × 66.7 )∶(3.30×50×10−3 )
S2Cl2
SO 2
135.2
100
=0.0829∶0.165=1∶1.99≈1∶2
∴S Cl +2SO +2H O === S O 2− +2Cl−+4H + 或
S2 Cl2 +2SO2 +2H 2 O === H 2 S4 O 6 +2HCl
(5)求无水钾盐(即 K2S4O6)与 KIO3 反应的物质的量之比,并书写反应式。
nS4 O62 −
∶nIO−
50.0 × 10−3
= ( 302.6
) ∶(23.2×.0.0250×10−3 )
=1.65×10−4∶5.8×10−4=2∶7.03≈2∶7
2S O2− +7IO − +7Cl− +10H+ === 7ICl+8HSO− +H O
4 6 3 4 2
 或
2K2S4O6+7KIO3+10HCl 7ICl+8KHSO4+3KCl+H2O
或
2K2S4O6+7KIO3+10HCl 7ICl+8KHSO4+3KCl+H2O
1987 年复赛试题
一、1.(2)>(3)>(1) 2.(2)>(1)>(3) 3.(1)>(3)>(2)
|
4.(1)>(2)>(3) 二、 |
5.(3)>(1)>(2) |
||
|---|---|---|---|
|
A、Cr2O3 |
B、CrCl3 |
C、Cl2 | D、K2Cr2O7 |
|
E、Cr2(SO4)3 |
F、NaCrO2 |
G、Na2CrO4 | |
|
H、Na2Cr2O7 |
I、H2CrO4(或 CrO5) |
J、Cr(OH)3 |
三、(1)室温下铜丝变黑反应如下:
1Cu(s) + O (g)→CuO(s)
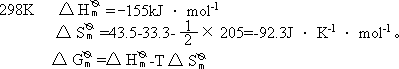 2
2
2
2
=−155−298×(−92.3)/1000=−127.5kJ·mol−1
<0
故在室温时上述反应自发进行。
1(2)2CuO(s) === Cu O(s) + O (g)
2 2 2
298K 时,△H
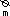 =0−167−2×
=0−167−2×
(−155)=143kJ·mol−1 △S∅=205× 1 +101-2×43.5=116.5J·K −1·mol −1。
3 2
∵△H
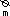 ,△S
,△S
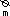 在相当宽的温度范围内,可视为基本不变。∴T
时,
在相当宽的温度范围内,可视为基本不变。∴T
时,
△G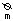 =143−T×116.5/1000,当△G
=143−T×116.5/1000,当△G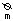 <0
时,该反应才能自发进行143−T × 116.5/1000<0,T>1227K
<0
时,该反应才能自发进行143−T × 116.5/1000<0,T>1227K

 四、
Zn+2NaNH2+2NH3 Na2Zn(NH2)4+H2↑ Zn(NH2)2− +2NH I Zn(NH )
↓(白)+4NH +2I− Zn(NH2)2+2NH4I■ZnI2+4NH3
四、
Zn+2NaNH2+2NH3 Na2Zn(NH2)4+H2↑ Zn(NH2)2− +2NH I Zn(NH )
↓(白)+4NH +2I− Zn(NH2)2+2NH4I■ZnI2+4NH3
 2.2Cu2++4I−
2CuI↓+I2
2.2Cu2++4I−
2CuI↓+I2
由于CuI是沉淀,则在溶液中[Cu + ]很小,致使
0.059
1
log
[Cu 2+ ]
[Cu + ] 值
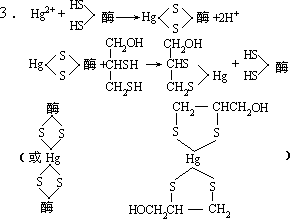 增大,所以ECu2
增大,所以ECu2
- /Cu + 值增大,使上述反应能够自发进行。
- 纠正酸中毒,补给 NaHCO3,过程如下:
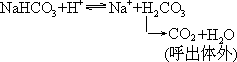
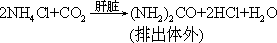
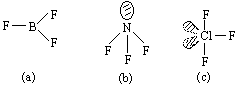 纠正碱中毒,补给
NH4Cl,大致过程如下:
纠正碱中毒,补给
NH4Cl,大致过程如下:
-
在 BF3 分子中,B 原子采取 sp2 杂化,3 个 sp2
杂化轨道在同一平面如同(a)。在 NF3 分子中,N 原子取不等性 sp3 杂化,杂化轨道间的夹角如图(b)。在 ClF3 分子中,Cl 原子取 sp3d 杂化,杂化轨道间的夹角如图(c)。(或用价层电子对互斥理论解释)。
-
BF3、BCl3、BBr3 均为平面形分子,在 BF3 分子中,B 原子的 2p
空
轨道与三个F原子的有孤对电子占据的2p轨道形成离域π键Π 6,使B原子的
缺电子情况大为改善。在BCl 分子中,这种Π 6很弱,B原子的缺电子情况
3 4
没有多少改善。在BBr 分子中,不存在这种Π6 键,因此,其中的B原子最易
3 4
接受电子对。
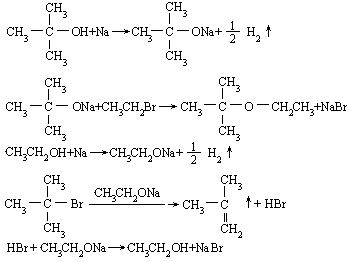 五、
五、
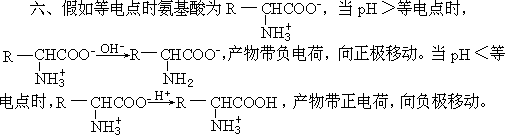
因此,缬氨酸,赖氨酸,谷氨酸带负电荷,向正极移动。丝氨酸 pH=1
<5.68,带正电荷,向负极移动。
