二、填空题
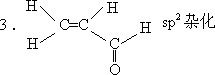 1.UF6
2.−519.7
1.UF6
2.−519.7
|
4.a.色散力 |
b.共价键 c.离子键 |
d.共价键和离子键 e.金 |
|
|---|---|---|---|
|
属键 |
f.共价键 |
5.Hg 6.不能 7. 2.0 ×10−10 8.逆 9. |
|
HI<NH4Br<KBr<NH3<KCN<NaOH |
10. 11.33 |
11.339.6 |
12.(a) |
|---|---|---|---|
|
0.0499≈0.05 (b) 0.075 |
13.8 种 3−甲基−2−丁醇和 2−戊醇(能 |
够氧化成羧酸的是)正戊醇、异戊醇、仲丁基甲醇、新戊醇(不能生成烯烃的是)新戊醇 14.CO2H H2C2O4
三、

C:乙醛 CH3CHO D:甲酸 HCOOH E:异丙醇(CH3)2CHOH
推导根据:(1)根据 A 的摩尔质量为 4.9×16=78 克/摩,以及燃烧产生浓烟,不与 KMnO4 和 Br2 水反应,可以判断 A 为苯;(2)根据 C 的摩尔质量为 2.75×16=44 克/摩,及有碘仿反应,必在α−C 上有三个 H,判断C 为乙醛,(3)B 有银镜反应,说明它含有醛基;它在碱性溶液中水解成小分子,可判断它为酯。而 D 和 E 分别为羧酸和醇。E(醇)在 I2−KI 的碱性溶液中被氧化成醛或酮,而后者又有碘仿反应,结合 B 的摩尔质量: 5.5×16=88 克/摩,则可判断 B 为甲酸异丙酯;E 为异丙醇;D 为甲酸。
四、
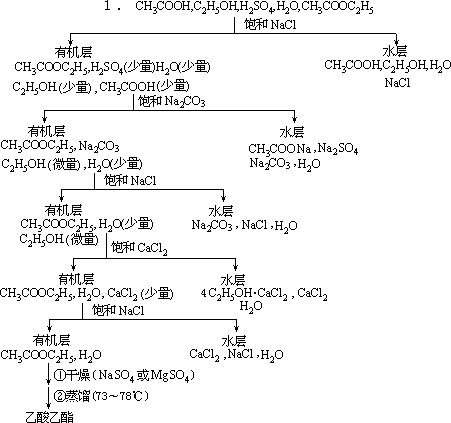
2.溶解顺序为:蒸馏水(溶解 KNO3)→氨水(溶解 AgCl)→NH4Ac 溶液(溶解 PbSO4)→(NH4)2S 溶液(溶解 SnS2)→热 HNO3 溶液(溶解 CuS)。
 五、A:碘化物(如
KI) B:浓 H2SO4 C:I2 D:I− E:S2O2− (如
Na2S2O3) F:Cl2
五、A:碘化物(如
KI) B:浓 H2SO4 C:I2 D:I− E:S2O2− (如
Na2S2O3) F:Cl2
反应方程式:
 1.8KI+9H2SO4(浓)
4I2+8KHSO4+H2S↑+4H2O
1.8KI+9H2SO4(浓)
4I2+8KHSO4+H2S↑+4H2O
2.I2+I−=I3−
3.I− +2S O 2− === S O 2− +3I−
4.I− +8Cl +9H O === 3IO − +16Cl− +18H+
5.S O 2− +2H + === SO +S↓+H O
2 3 2 2
6.4Cl +S O 2− +10OH − === 2SO2− +8Cl− +5H O
2 2 3 4 2
7.SO2− +Ba 2+ === BaSO ↓
六、1.VO 3− +4H+ === VO + +2H O (1)
2VO + +SO
=== 2VO 2+ +SO2−
(2)
5VO 2+ +MnO− +H O === 5VO + +Mn2+ +2H+
2.根据方程式(3)可知 VO2+的物质的量为:
(3)
n(VO2+)=5×18.73×23.2×10−6/1=2.173×10−3(mol)
由方程式(1)(2)可知:
n(VO 3− ) = n(VO + ) = n(VO2+ ) = 2.173×10−3 (mol)
钒酸铵的浓度为:
C(NH4)3VO4=(2.173×10−3/25.0)×106=86.9(mol·m−3)
- 钒酸铵溶液酸化后被锌汞齐还原,所得含钒物种(紫色)的物质的量与原始钒酸铵(NH4)3VO4 物质的量相等,即为:
n=86.9×10×10−6=8.69×10−4(mol)
设该紫色含钒物种 V 的化合价为+n,则在酸性条件下,它被 KMnO4 氧化为
VO + ,MnO− 被还原为Mn2+ ,根据氧化 - 还原反应中氧化剂与还原剂化合价
2 4
改变相等的原则,得出紫色含钒物种与 KMnO4 在酸性溶液中反应的物质的量之比为:5∶(5−n)
∴(5−n)×8.69×10−4=5×18.73×27.8×10−6 (5−n)=2.60×10−3/8.69×10−4=2.99
n=2
- 根据两次滴定数据分析,确定第一次滴定的是VO 2+ 和C
O2− ,第
二次滴定的是 VO2+,因此计算过程如下:
蓝色络合物的摩尔质量 M=(14.0+1.01×4)x+50.9+16.0+(12.0× 2+16.0×4)y+(16.0+1.01×2)×
 2=18.0x+88.0y+102.9
18.0x+88.0y+103
2=18.0x+88.0y+102.9
18.0x+88.0y+103
5VO 2+ + H O + MnO− === 5VO+ + Mn 2+ + 2H+
5
237.4 × 10−3
1
19.4×7.8×10−6
103 + 18.0x + 88.0y
∴ 237.4×10−3×1/[103+18.0x+88.0y]=7.8×10−6×19.4×5 整理得:18.0x+88.0y=210.8 (1)
5C O 2− + 16H + + 2MnO− === 2Mn2+ + 10CO ↑ + 8H O
2 4 4 2 2
5 2
237.4 × 10−3 y −
103 + 18.0x + 88.0y
19.4×(38.95 - 7.80)×10 6
∴ 2×237.4×10−3y/[103+18.0x+88.0y]
=5×19.4×(38.95−7.80)×10−6
整理得:18.0x−69.1y=−103 (2) (1)−(2):157y=313.8
y≈2.00 x=1.93≈2.0
∴x=2,y=2 1989 年竞赛试题
|
一、选择题 |
||||
|---|---|---|---|---|
|
1.(A,C) |
2.(B) |
3.(C) |
4.(B) |
5.(B) |
|
6.(B) |
7.(C) |
8.(C) |
9.(C) |
10.(C) |
|
11.(A) |
12.(D) |
13.(C) |
14.(D) |
15.(C) |
16.(C) 17.(A) 18.(B, D) 19.(C) 20.(A,
B)
21.(A,C) 22.(A,D) 23.(E) 24.(D) 25.(D)
二、选择题 1.(C) 2.(B) 3.(B) 4.(A) 5.(D) 三、填空题
1.3 2.C2H4 3.33—34%范围值都正确
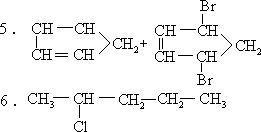
 4.5RuS2+4KClO3+6HCl
3RuO4+2RuCl3+3H2S+7S+4KCl
4.5RuS2+4KClO3+6HCl
3RuO4+2RuCl3+3H2S+7S+4KCl
