二、选择题(22 分)
下列各题可能有 1~2 个正确答案,也可能没有正确答案。有正确答案者,将其标号(A、 B、 C、 D、 E)填入括号内;没有正确答案者,则填写“×”号。若试题只有一个正确答案,选答两个者不给分; 若试题有两个答案者,全对才给分。
-
电子层结构为[Ar]3d6 的离子是 [ ] A.Mn2+ B.Fe3+ C.Co3+ D.Ni2+
-
下列微粒中与 NH+4 离子的质子总数和电子总数都相同的是[ ]
A.Mg2+ B.K+ C.Na+ D.Ne E.H3O+
|
3.1 克下列气体,在标准状况下占据最大体积的是 |
[ |
] |
|---|---|---|
|
A.乙烷 B.氟气 C.硫化氢 D.氧气 |
E.氖气 |
|
|
4.下列气体中,对热最不稳定的是 A.H2O B.H2S C.PH3 D.HF |
[ |
] |
|
5.下列各组物质,不属于同素异形体的是 |
[ |
] |
A.红磷与白磷 B.水和重水
C.16O 与 18O D.氧气与臭氧(O3) 6.下列实验事实能证明硫酸是强酸的是 [ ]
A.使石蕊试纸变红 B.和铜反应 C.与锌反应产生氢气 D.与氯化钠固体反应制取氯化氢E.与磷酸钙反应制取磷酸
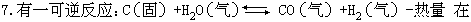
某温度下达到平衡。下列说法中正确的是 [ ] A.达到平衡时,各反应物与生成物浓度一定相等 B.升高温度,使正向反应速率增大,逆向反应速率减小,故平衡向右移动C.由于反应前后分子数相等,所以增加压力对平衡无影响 D.加入正催化剂使正向反应速率增大,故平衡向右移动
8.在一定条件下进行的下列反应中,既不是氧化—还原反应,又不是水解反应的是 [ ]


 C.SO2−3+H2O
HSO−3+OH− D.CO+H2O CO2+H2
C.SO2−3+H2O
HSO−3+OH− D.CO+H2O CO2+H2
- mol·dm−3 碳酸钠溶液中,欲使[CO2−3]接近 0.1mol·dm−3,则应向溶液中加入或通入 [ ]
A.NaOH B.CO2 C.HCl D.NaCl 溶液
10.把铁片投入下列溶液中,(必要时加热),铁片溶解,且没有气
|
体产生的是 |
[ |
] |
|---|---|---|
| A.H2SO4 B.Al2(SO4)3 | ||
| C.FeSO4 D.Fe2(SO4)3 | ||
|
11.下列溶液中 pH 值最小的是 |
[ |
] |
|
pH 值最大的是 A.0.1mol·dm−3Hac B.0.01mol·dm−3HAc C.0.1mol·dm−3H3PO4 D.0.01mol·dm−3H3PO4 |
[ |
] |
E.0.1mol·dm−3HCl F.0.1mol·dm−3H2SO4 12.下列说法正确的是 [ ]
A.将 NaOH 和氨水溶液各稀释一倍,则两者的 OH−离子浓度均减小到原来的二分之一
B.HCl 溶液的浓度是 HAc 溶液浓度的二倍,则 HCl 溶液中[H+]也为 HAc 溶液中[H+]的二倍
C.中和等体积同浓度的 HCl 和 HAc 溶液所需要的碱量相等D.弱酸的浓度越小,其电离度也越大,所以酸性也越强
- 胶体区别于其它分散系的本质特征是 [ ] A.胶体微粒带电荷
B.分散质微粒直径在 10−9−10−7m 之间C.可产生了铎尔现象 D.胶体微粒做布朗运动 E.胶体微粒不能穿过半透膜
- 用石墨电极电解下列溶液,一段时间后阴极增重,溶液 pH 值降低的是 [ ]
A.H2SO4 B.MgCl2 C.KOH D.CuSO4 E.CuCl2 15.氢气和一氧化碳的混合气体 30cm3,完全燃烧共用去氧气 15cm3,
此混合气体中氢气和一氧化碳的体积比是 [ ]
A.1∶1 B.2∶1
C.3∶1 D.任意比 E.以上都不对
- 浓度为 0.1mol·dm−3 某一元弱酸 HA,其 pH 值等于 3,该酸在
0.1mol·dm−3 时的电离度为 [ ] A.0.01% B.0.3% C.1% D.3% E.9%
- 在标准状况下,13 克某气体的分子数与 14
克乙烯的分子数相等,则某气体的密度是 [ ]
A.11.6 克/分米 3 B.1.16 克/厘米 3
C.1.16 克/分米 3 D.1.25 克/分米 3
E.1.25 克/厘米 3
18.0.2mol·dm−3Al2(SO4)3 溶液 100cm3 与 0.3mol·dm−3(NH4)2SO4 溶液 200cm3 混合后,需至少加入 0.4mol·dm−3NaOH 溶液多少 cm3 便仍可得
|
到澄清溶液 |
[ |
] |
|||
|---|---|---|---|---|---|
|
A.350 |
B.400 |
C.550 |
D.700 |
E.850 |
