第一节 氢气的实验室制法
制取氢气的实验
人类制取氢气,最先是采用铁和稀硫酸作用。直到现在,在实验室里, 仍然用金属跟酸反应来制取氢气。让我们用自制的氢气充一个气袋。
[实验 5—1]取一支大试管加入一些锌粒和约 1/4 容积的稀硫酸,塞好带导管的橡皮塞。把薄膜塑料袋套在塞子的导管上,观察锌粒表面发生的现象和塑料袋体积的变化。把塑料袋口用细线扎紧,拔下导管,气袋能升空吗?由实验可见,用稀硫酸和锌反应,能制得氢气。那么,溶液中有没有其
它物质生成呢?
[实验 5—2]用玻璃棒蘸取实验 5—1 反应后的溶液,。滴在玻璃片上, 然后在酒精灯焰上方烘烤,观察玻璃片上留下的物质的颜色和状态。
玻璃片上有白色固体物质出现,这是反应生成的另一种物质——硫酸锌(ZnSO4)。锌和稀硫酸反应制取氢气的化学方程式为:
Zn+H2SO4=ZnSO4+H2↑
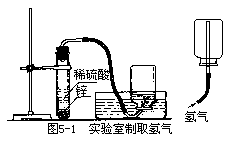
【想一想】实验室制取少量氢气时,常用图 5—1 所示的装置。你能说出这套装置中各种仪器的名称吗?
[实验 5—3]用图 5—1 所示的装置制取氢气。将锌粒放在大试管中, 加入稀硫酸至液面覆盖住锌粒,塞好橡皮塞,观察反应现象。先用排水法收集一瓶氢气,用毛玻璃片盖住集气瓶口,倒放在桌面上。再用向下排空气法(如图 5—1 右)收集一瓶氢气,也用毛玻璃片盖住集气瓶口,倒放在桌面上。观察氢气的颜色和状态。
【议一议】(1)在收集氢气时使用的两种方法,各说明氢气有什么性质?
(2)盛有氢气的集气瓶为什么要倒放在桌面上?
工业上所用的大量氢气,除常用水煤气(主要成分是一氧化碳和氢气)、天然气(主要成分是甲烷)等来制取外,还可通过电解水来制取。
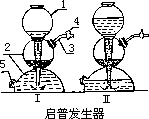
【选学】在实验室里,需要制取较多氢气时,常使用启普发生器。
启普发生器是由荷兰人启普(1808~1864)设计的,它由球形漏斗 1、容器 2 和导气管 3 三部分组成。使用时首先拔下带导气管的橡皮塞,将锌粒加在容器的球体下部,再塞上橡皮塞。然后旋开导气管活塞 4,从球形漏斗口加入酸,酸液顺漏斗流下,在容器内与锌粒接触,发生反应,产生的氢气从导气管放出(如图Ⅰ)。不用时关闭导气管活塞,容器内压强加大,把酸液压回球形漏斗里,使酸与锌粒脱离接触,反应即自行停止(如图Ⅱ)。用启普发生器制取氢气,可以随时使反应发生,也可以随时使反应停止,使用起来既方便又节省药品。
【练一练】与锌跟稀硫酸反应相似,锌还能跟盐酸(HCl)反应,镁也能跟稀硫酸、盐酸反应。试写出镁跟稀硫酸、锌跟盐酸反应的化学方程式。
镁跟稀硫酸反应的化学方程式为:
Mg+H2SO4= MgSO4+H2↑ 锌跟盐酸反应的化学方程式为:
Zn+2HCl=ZnCl2+H2↑
分析锌、镁跟稀硫酸、盐酸的反应,可以看出这些反应与化合反应、分解反应不同,参加反应的物质是一种单质和一种化合物,生成的物质是另一种单质和另一种化合物。这类由一种单质跟一种化合物反应,生成另一种单质和另一种化合物的反应,叫做置换反应。
我们学过的化合反应、分解反应和置换反应,都是化学反应的基本类型。
根和根价
在锌跟稀硫酸的反应中,硫酸分子(H2SO4)中的“SO4”部分,好像一个原子一样,反应后转入硫酸锌中。像这种由几个原子结合的集团,叫做原子团,也称为“根”。例如,硫酸(H2SO4)中的“SO4”叫做硫酸根,氢氧化钙
[Ca(OH)2]中的“OH”叫做氢氧根,碳酸钙(CaCO3)中的“CO3 ”叫做碳酸根,等等。
根与某些元素的原子结合可组成化合物,因此根也有化合价。根的化合
价称为根价。由于根是由几个原子结合而成的,我们可根据组成根的各元素的化合价来计算根价。
根价等于其所含各元素化合价的代数和。例如,硫酸根中硫元素的化合价为+6,氧元素的化合价为-2,则硫酸根的化合价为:
(+6) ×1+(-2)×4=(+6)+(-8)= -2。
根价也可利用化学式中其它元素的化合价计算。例如,在 Na2SO4 中 Na 为+1 价,则
(+1)× 2+SO4 的化合价=0
SO4 的化合价=-2
我们知道,带电荷的原子称为离子。同样,带电荷的根也是离子。例如, 硫酸根离子( SO42-)、碳酸根离子( CO32-)、硝酸根离子( NO3-)、氢氧根离子( OH-)等。显然,根离子所带的电荷数应等于根的化合价数值。
根据根价,可以写根与原子或其它根组成的化合物的化学式。
【练一练】已知铜的化合价为+2,铁的化合价为+3,分别写出铜与氢氧根、铁与硫酸根组成的化合物的化学式。
